
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
6.5. Изучение закономерностей процесса вымораживания солей из модельных растворов
В предыдущей главе установлено, что на процесс вымораживания высокоминерализованных растворов основное влияние оказывают температурный режим, состав и структурные характеристики растворов; температуры замерзания концентрированных растворов солей являются аномально пониженными. Были установлены изменения характера зависимости вязкости, электропроводности, химического сдвига от концентрации. При минерализациях 300 и 460 г/дм3 происходит резкое (скачкообразное) изменение свойств рассолов, свидетельствующее о структурных преобразованиях растворителя.
Изучение возможности опреснения проводили методом вымораживания на растворах, моделирующих реальные рассолы. Исходный состав модельных растворов представлен в таблице 13.
Таблица 13. Содержание элементов в модельных растворах
| Номер модельного раствора (общее солесодержание) | Содержание элементов, г/дм3 | |||||
| Ca | Na | Cl | Sr | Li | Br | |
|
0 (264 г/дм3) |
84,77 |
25 |
150 |
1,5 |
0,25 |
3 |
|
1 (134 г/дм3) |
42,39 |
12.5 |
75 |
1,5 |
0,25 |
3 |
|
2 (80 г/дм3) |
21,19 |
6,25 |
37,5 |
1,5 |
0,25 |
3 |
|
3 (70 г/дм3) |
21,19 |
6,25 |
37,5 |
0,53 |
0,25 |
3 |
|
4 (68 г/дм3) |
21,19 |
6,25 |
37,5 |
0,26 |
0,25 |
3 |
Результаты замораживания в морозильной камере показали, что в течение 1 часа полностью перешли в твёрдую фазу (лёд) пробы 1-4, раствор с минерализацией 264 г/дм3 не кристаллизуется (температура замерзания этого раствора равна -24,8°С, формула выведена во 2 главе). Температуры замерзания растворов 1-4 следующие: -9,4; -5,1; -4,4; -4,2 , соответственно. Для установления распределения общего солесодержания в ледяной фазе были отобраны три пробы в процессе таяния льда, время отбора проб через каждые 10 мин. после начала таяния (табл.14). Полученные данные свидетельствуют о том, что во время размораживания происходит опреснение льда. Наиболее концентрированный раствор получается в первых пробах тающего льда, наименее концентрированный - в последних.
Таблица 14. Солесодержание ледяной фазы в процессе таяния льда
|
№ пробы |
Минерализация исходного раствора, г/дм3 |
Минерализация в пробах ледяной фазы, отобранных в процессе таяния льда, г/дм3 |
||
|
1 проба |
2 проба |
3 проба |
||
|
1 |
134 |
145,62 |
116,01 |
71,87 |
|
2 |
80 |
101,6 |
78,24 |
31,94 |
|
3 |
70 |
99,6 |
69,5 |
43,08 |
|
4 |
68 |
91,44 |
68,78 |
42,46 |
Результаты вымораживания показали, что для концентрированных рассолов, чем больше минерализация исходного раствора, поступающего на вымораживание, тем менее минерализованный лёд можно получить (Рис. 51).
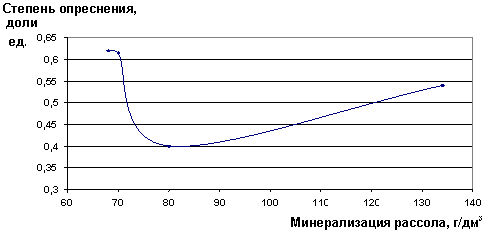
Рис. 51. Зависимость степени опреснения льда от минерализации
Установлено, что степень концентрирования раствора наибольшая там (рис. 52), где меньше общая минерализация исходного раствора. Чем больше исходная минерализация рассола, тем меньше будет разница в минерализациях исходного раствора и раствора, сконцентрированного замораживанием, тем преснее лёд.
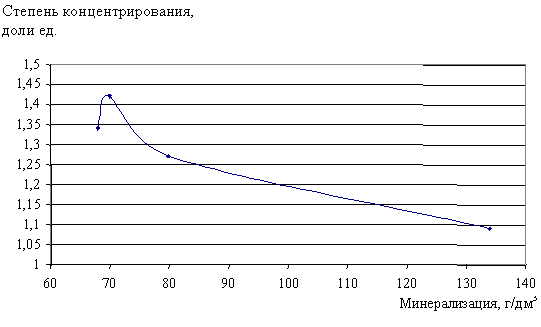
Рис. 52. Зависимость степени концентрирования раствора от исходной минерализации
Определение действительного состава модельных растворов произведено с помощью термодинамического моделирования. Содержание свободных ионов и ассоциатов представлено на диаграммах (рис. 53-54).
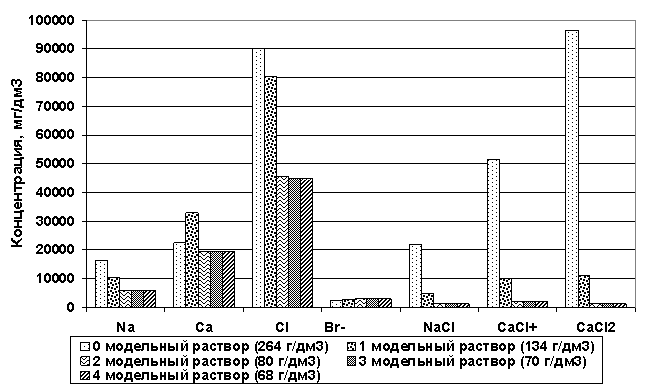
Рис. 53. Действительный состав модельных растворов (макрокомпоненты)
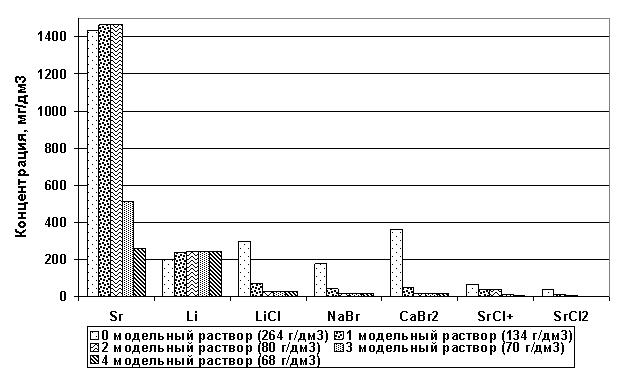
Рис. 54. Действительный состав модельных растворов (микрокомпоненты)
Видно, что в модельных растворах преобладают макрокомпоненты - ионы Na+, Ca2+, Cl-, Br- и ассоциаты - NaCl, CaCl+ и CaCl2. Микрокомпоненты в растворах находятся в виде Sr2+, Li+, LiCl, NaBr, CaBr2, SrCl+, SrCl2. Можно отметить, что с повышением общей минерализации раствора увеличиваются концентрации ассоциатов. Ионы кальция в растворах высоких минерализаций склонны к образованию ассоциатов и ионных комплексов более, чем другие компоненты раствора. С увеличением минерализации раствора больше ионов кальция оказывается связанным.
Процентное содержание свободных ионов в растворах показывает, какие ионы в большей степени способны к связыванию в ассоциаты, комплексы, а какие остаются в свободной форме до очень высоких минерализаций. Из диаграмм на рис. 55-56 видно, что кальций, натрий и хлор больше склонны к образованию комплексов, тогда как стронций и литий практически полностью находятся в свободном состоянии. Данный факт необходимо учитывать при разработке технологических схем извлечения ценных компонентов из рассолов.
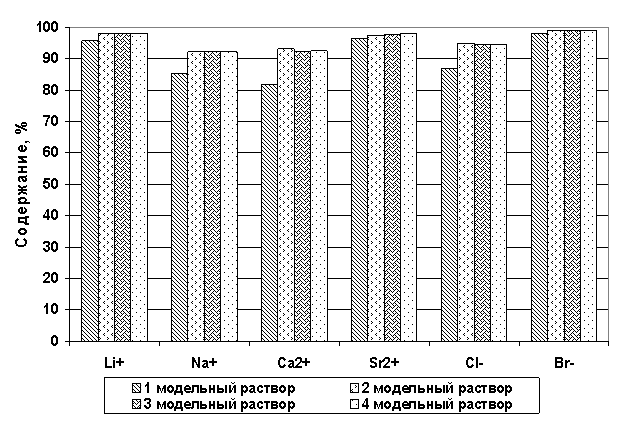
Рис. 55. Процентное содержание свободных ионов в модельных растворах
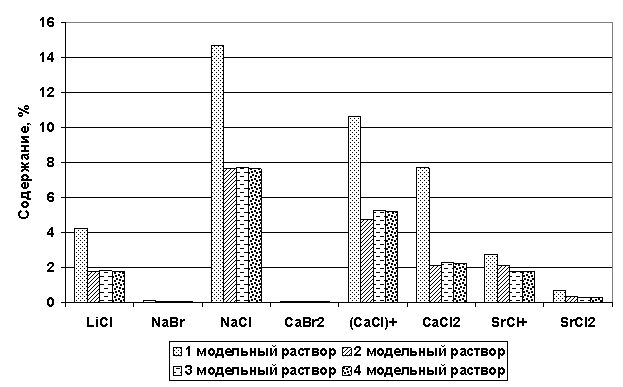
Рис. 56. Процентное содержание ассоциатов в модельных растворах
Так как раствор с минерализацией 264 г/дм3 не замёрз при температуре минус 20°С, а остальные растворы замёрзли, то мы полагаем, что структура и концентрация раствора здесь оказала решающее значение. В данном растворе много ассоциатов и комплексов (особенно велика доля соединений кальция - а температура замерзания хлоридно-кальциевых растворов сама по себе достаточно низкая), что значительно снижает температуру замерзания растворов.
Быстрее замерзают растворы, в которых компоненты находятся в форме свободных ионов. При увеличении концентрации составляющих раствор компонентов они начинают связываться в соединения, ассоциаты и комплексы. Поэтому чем менее концентрирована исходная система, тем большую температуру замерзания она имеет и тем проще её заморозить.
