
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
3.1 s-элементы
3.1. s-элементы I группы при их окислении свободным кислородом наряду с нормальными оксидами Э2О имеют склонность к образованию пероксидов Э2О3, надпероксидов ЭО2, и озонидов ЭО3, однако стремление к образованию более богатых кислородом соединений выражено у них в разной степени и может быть количественно оценено величиной (ΔG°298) образования кислородных соединений.
На основании значений (ΔG°298)обр кДж/2 моль металла различных кислородных соединений щелочных металлов, приведенных в табл. 16 определите, образование каких соединений наиболее характерно для различных щелочных металлов.
Таблица 16
|
Элемент |
Э2О(Т) |
Э2О2(Т) |
ЭО2(Т) |
ЭО3(Т) |
|
Li |
- 560 |
- 564 |
- 468 |
- |
|
Na |
- 376 |
- 439 |
- 433 |
- |
|
K |
- 322 |
- 422 |
- 475 |
- 380 |
|
Rb |
- 290 |
- 351 |
- 439 |
- 577 |
|
Cs |
- 290 |
- 332 |
- 418 |
- 577 |
Чем можно объяснить наблюдаемые закономерности?
3.2. Элементы подгруппы Be образуют с кислородом оксиды ЭО и пероксиды ЭО2. (ΔG°298)обр, кДж/моль, кислородных соединений этих элементов имеют значения, указанные в табл. 17.
Таблица 17
|
Оксиды |
Ве |
Mg |
Ca |
Sr |
Ba |
|
ЭО(Т) |
- 599 |
- 602 |
- 635 |
- 591 |
- 559 |
|
ЭО2(Т) |
- |
- 623 |
- 654 |
- 641 |
- 636 |
На основании приведенных данных ответьте на следующие вопросы:
а) Какие из s-элементов II группы преимущественно образуют оксиды; пероксиды?
б) Какой из рассматриваемых элементов обладает наибольшим сродством к кислороду?
в) Оцените методом экстраполяции (ΔGо298)обр оксида и пероксида радия, построив для этого график изменения (ΔGо298)обр ЭО и ЭО2 в зависимости от атомного номера элемента.
3.3. Способность оксидов s-элементов образовывать основания можно количественно оценить величиной ΔGо298 реакций:
Э2O(Т) + H2O(Ж) = 2ЭOH(Т);
ЭO(Т) + H2O(Ж) = Э(OH)2(Т);
Пользуясь справочными данными, вычислите ΔGо298 для s-элементов I и II групп.
а) На основании справочных данных по энергиям связи Э - О качественно оцените сравнительную силу оснований ЭОН и Э(ОН)2. Наблюдается ли корреляция между значениями ΔGо298 приведенных реакций и основными свойствами гидроксидов?
б) Как и почему изменяются основные свойства оксидов в каждой подгруппе с ростом атомного номера элемента?
в) Сопоставьте проявление основного характера оксидов s- элементов I и II групп. Оксиды элементов какой группы и почему образуют более сильные основания?
г) Как изменяется термическая устойчивость гидроксидов ЭОН и Э(ОН)2 в отношении их распада на соответствующий оксид и воду в пределах, каждой подгруппы с увеличением атомного номера?
д) Какие гидроксиды и почему термически более устойчивы: ЭОН или Э(ОН)2?
3.4. Известно, что ион аммония NH4+ во многих отношениях имеет свойства, близкие свойствам ионов s-элементов первой группы, особенно К+.
Приведите как можно больше примеров как сходства, так и различия физико-химических свойств этих ионов и содержащих их соединений. С чем можно связать сходство рассматриваемых ионов?
3.5. Для описания поведения иона в водном растворе применяется параметр, называемый подвижностью и характеризующий скорость движения иона вдоль поля, напряженность которого равна 1 В/см. Подвижность иона в первую очередь зависит от его радиуса: чем меньше радиус, тем подвижность иона больше.
В табл. 18 представлены численные значения подвижностей ионов щелочных металлов и их энергий гидратации.
Таблица 18
|
Параметры |
LI+ |
Na+ |
K+ |
Rb+ |
Cs+ |
|
Энергия гидратации, кДж/моль |
520 |
405 |
322 |
300 |
255 |
|
Подвижность, Ом-1, см |
33 |
44 |
65 |
67 |
68 |
а) Почему подвижность ионов при переходе от лития к цезию возрастает, несмотря на увеличение ионного радиуса в этом же ряду?
б) Как связать увеличение подвижности ионов щелочных металлов с атомным номером и уменьшением энергии гидратации в этом же ряду?
в) Почему самому маленькому иону (Li+) соответствует наименьшая подвижность и наибольшая энергия гидратации?
3.6. Химическая активность щелочных металлов закономерно возрастает с увеличением атомного номера элемента: наиболее химически активен из них цезий, наименее - литий. Стандартные электродные потенциалы щелочных металлов в водных растворах имеют следующие значения, В:
Li+ /Li Na+ /Na K+ /K Rb+ / Rb Cs+ /Cs
- 3,04 - 2,71 - 2,91 - 292 - 292
а) Чем объяснить, что не цезий, и литий в водных pастворах является наиболее сильным восстановителем?
б) Почему стандартные электродные потенциалы рубидия и цезия одинаковы?
3.7. Вычислите ΔG298 для реакций термического разложения карбонатов s- элементов II группы по реакции ЭСО2 = ЭО + СО2 на основании справочных данных.
Рассчитайте температуры начала термического разложения (Тр) карбонатов этих элементов и сделайте вывод об изменении их термической устойчивости в зависимости от атомного номера. Как объяснить полученные результаты?
Постройте график зависимости Tp = f(Za - атомный номер). Методом экстраполяции определите Тр радия.
3.8. Металлические свойства s-элементов I группы от лития к цезию возрастают, а электропроводность металлов в этом же ряду уменьшается. С чем это можно связать?
3.9. Важной характеристикой простых катионов является их ионный потенциал - отношение заряда иона к его радиусу.
Пользуясь справочными данными, рассчитайте ионные потенциалы для s-элементов II группы. Какие из этих ионов должны иметь наибольшее сходство с Ga3+ и Аl3+? В чем проявляется это сходство?
3.10. На примере орбитальных атомных и ионных (Ме+ и Me2+) радиусов, потенциалов ионизации (I1 для элементов первой группы и I1 + I2 для элементов второй группы) и стандартных энтропий газообразных атомов исследуйте наличие или отсутствие проявлений вторичной периодичности свойств s-элементов, построив соответствующие графики зависимостей указанных параметров от атомного номера элемента.
Дайте объяснение особенностей хода кривых. Для ответа на вопрос воспользуйтесь справочными данными приложения.
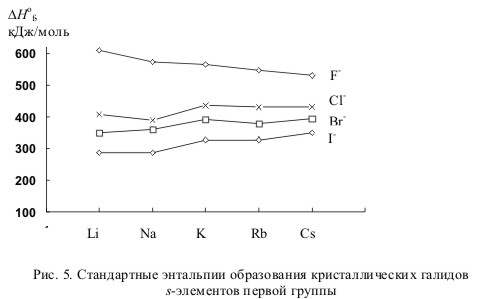
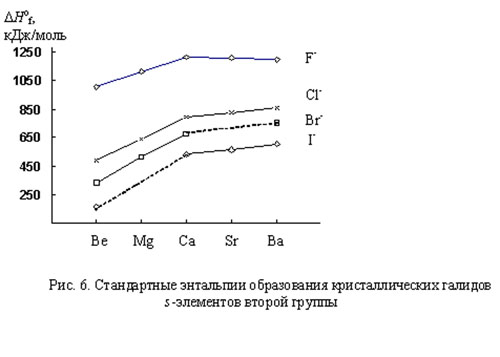
3.11. Ниже представлены зависимости стандартных энтальпий образования кристаллических галидов s-элементов первой (рис. 5) и второй (рис. 6) групп.
а) Как и почему изменяется термическая устойчивость галидов в рядах МеF - МеI и MeF2 - MeI2?
б) Чем объяснить особенно высокую термическую устойчивость фторидов металлов обеих подгрупп по сравнению с остальными галидами?
в) Почему термическая устойчивость фторидов щелочных металлов монотонно уменьшается в ряду LiF-CsF, тогда как для остальных галидов этих элементов наблюдается тенденция к увеличению устойчивости в этом же ряду?
г) Как можно объяснить аномально низкую устойчивость иодида цезия?
д) Проанализируйте график зависимости энтальпий образования галидов s-элементов второй группы (рис. 6): 1) Почему на всех кривых наблюдается излом на галидах кальция? 2) Чем объяснить некоторое снижение термической устойчивости фторидов в ряду. СаF-ВаF2,, тогда как для остальных галидов в этом же ряду наблюдается монотонное увеличение энтальпии образования? 3) Данные для энтальпии образования иодида магния в справочной литературе отсутствуют. Оцените эту величину методом интерполяции.
е) Сравните графики обоих рисунков и дайте сравнительный анализ хода аналогичных кривых для элементов первой и второй групп с объяснением сходства и различия термических характеристик галидов элементов этих двух групп.
3.12. Стандартные электродные потенциалы (Еo, В) s-элементов второй группы в водных растворах имеют следующие значения:
Be2+/Be Mg2+/Mg Са2+/Са Sr2+/Sr Ba2+/Ba Ra2+/Ra
- 1,85 - 2,37 - 2,87 - 2,89 - 2,90 - 2,92
а) Объясните причину последовательного усиления воcстановительной активности металлов с точки зрения особенностей их электронного строения.
б) Стандартный окислительно-восстановительный потенциал полуреакции восстановительного разложения воды 2Н2О + 2е = Н2 + 2ОН- при рН 7 равен - 0,41 В. Какие металлы способны взаимодействовать с водой по реакции
Me(T) + 2H2O(Ж) = Me(OH)2(Т) + Н2(г)
в) Вычислите ∆G0298 для реакций взаимодействия металлов с водой. Согласуются ли полученные значения с ответом на вопрос б)? Как изменяются восстановительные свойства металлов в зависимости от атомного номера?
г) Почему, несмотря на отрицательные значения Е° и ΔG°298, бериллий и магний при обычных условиях не взаимодействуют с водой?
д) Представьте графически зависимость стандартного электродного потенциала от атомного номера элемента. Почему потенциалы металлов от кальция до радия лежат практически на одной прямой, что свидетельствует о близости cвойств этих металлов? Дайте ответ на основании особенностей электронного строения элементов.
е) Ниже приведены энергии гидратации ионов s-элементов второй группы ΔG h°, кДж/моль:
Ве2+ Mg2+ Ca2+ Sr2+ Ba2+ Rа2+
-2407 -1840 -1517 -1385 -1261 -1232
Представьте графически зависимость энергии гидратации от атомного номера элемента и сопоставьте полученный график с тем, который Вы построили в пункте д) задачи. Что можно сказать о влиянии гидратации катионов на величину стандартного электродного потенциала металлов? Обратите внимание на то, что, как и в предыдущем пункте, для металлов от кальция до радия наблюдается монотонная зависимость (соответствующие точки практически укладываются на прямую линию).
3.13. Рассмотрите изменение растворимости в воде сульфатов и гидроксидов по ряду Mg-Са-Sr-Ва и определите, каким (большим или меньшим) будет значение растворимости соответствующих соединений радия по сравнению с аналогичными соединениями бария.
