
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
3.4 f-элементы
3.47. В табл. 32 и рис. 7 приведены некоторые свойства лантаноидов.
а) Как можно объяснить нерегулярности в заполнении электронных оболочек у лантаноидов?
б) Чем обусловлено очень большое сходство свойств лантаноидов и лантана?
Таблица 32
|
№ |
Элемент |
Электронная конфигурация |
Орбитальный атомный радиус, |
Орбитальный радиус иона Ln3+, |
Ln3+/Ln2+, В (эксперимент) |
Ln3+/Ln, В (эксперимент) |
|
57 |
La |
5d16s2 |
1,915 |
0,819 |
- |
- 2,52 |
|
58 |
Ce |
4f26s2 |
1,978 |
0,800 |
- 2,92 ± 0,08 |
- 2,48 |
|
59 |
Pr |
4f36s2 |
1,942 |
0,783 |
- 2,84 ± 0,06 |
- 2,46 |
|
60 |
Nd |
4f46s2 |
1,912 |
0,767 |
- 2,62 ± 0,05 |
- 2,43 |
|
61 |
Pm |
4f56s2 |
1,882 |
0,751 |
- 2,44 ± 0,05 |
- 2,42 |
|
62 |
Sm |
4f66s2 |
1,854 |
0,737 |
- 1,50 ± 0,01 |
- 2,41 |
|
63 |
Eu |
4f76s2 |
1,826 |
0,723 |
- 0,31 ± 0,01 |
- 2,40 |
|
64 |
Gd |
4f75d16s2 |
1,713 |
0,710 |
- 2,85 ± 0,07 |
- 2,40 |
|
65 |
Tb |
4f96s2 |
1,775 |
0,698 |
- 2,83 ± 0,07 |
- 2,39 |
|
66 |
Dу |
4f106s2 |
1,750 |
0,686 |
- 2,56 ± 0,05 |
- 2,35 |
|
67 |
Ho |
4f116s2 |
1,727 |
0,674 |
- 2,79 ± 0,06 |
- 2,32 |
|
68 |
Er |
4f126s2 |
1,703 |
0,664 |
- 2,87 ± 0,08 |
- 2,30 |
|
69 |
Tm |
4f136s2 |
1,681 |
0,652 |
- 2,22 ± 0,05 |
- 2,28 |
|
70 |
Yb |
4f146s2 |
1,658 |
0,642 |
- 1,18 ± 0,01 |
- 2,27 |
|
71 |
Lu |
4f145d16s2 |
1,553 |
0,632 |
- |
- 2,25 |
|
Степень окисления
окисления |
La |
Ce |
Pr |
Nd |
Pm |
Sm |
Eu |
Gd |
Tb |
Dy |
Ho |
Er |
Tm |
Yb |
Lu |
|
1 |
|
|
|
|
|
? |
? |
|
|
|
|
|
|
|
|
|
2 |
|
× |
× |
× |
× |
II |
= |
× |
× |
× |
× |
× |
II |
II |
|
|
3 |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
= |
|
4 |
|
II |
II |
II |
|
|
|
|
× |
× |
|
|
II |
|
|
Рис. 7. Степени окисления лантаноидов: X - неустойчивые; = - устойчивые;
II - наиболее устойчивые
в) Из рис. 7 следует, что для большинства лантаноидов наиболее характерная степень окисления равна 3+.Объясните этот факт.
г) Изобразите графически зависимость орбитальных атомных радиусов и орбитальных радиусов ионов Ln3+ or порядкового номера элемента. Сопоставьте полученные графики. Как объяснить немонотонности на одном из них и отсутствие таковых на другом? С чем связана общая тенденция, наблюдаемая на обоих графиках - уменьшение радиусов с ростом порядкового номера?
д) В ряду лантаноидов наблюдается внутренняя периодичность. Установлено, что элементы от Рr do Eu во многих отношениях сходны с элементами от Dy до Yb. Как можно объяснить наличие внутренней периодичности, основываясь на электронном строении атомов и имея, в частности, в виду определенную симметрию распределения электронов (какую?) в пáрах Ce-Er, Pr-Ho, Nd-Dy, Pm-Tb, Eu-Yb?
Проиллюстрируйте проявление внутренней периодичности в ряду лантаноидов, например, ходом кривых зависимости стандартных окислительно-восстановительных потенциалов Е° Ln3+/Ln2+ от порядкового номера элемента. Аналогичные кривые постройте для энергий атомизации, температур плавления и кипения простых веществ. Прокомментируйте ход кривых.
е) Что можно сказать о химической активности лантаноидов в свободном состоянии, судя по их стандартным электродным потенциалам Е° Ln3+/Ln2+? Способны ли эти металлы взаимодействовать с водой и кислотами? Какой из металлов должен наиболее энергично разлагать воду? Напишите уравнения его взаимодействия с водой и серной кислотой.
ж) Какими кислотно-основными свойствами должны обладать оксиды Ln2O3 и гидроксиды Ln(ОН)3 и как эти свойства должны изменяться в ряду от церия до иттербия? Приведите уравнения реакций, иллюстрирующие Ваш ответ.
з) Объясните тот факт, что соединения LnI2 (Ln = La, Ce, Pr, Gd, Dy) обладают металлической проводимостью, сопоставимой с проводимостью натрия и калия. Какова степень окисления атомов металлов в этих соединениях?
3.48. Одним из важнейших вопросов химии f-элементов является выяснение их возможных степеней окисления. Известно (см. табл. 32 и рис. 7), что большая часть лантаноидов имеет электронную конфигурацию 4fn6s2, исходя из чего можно предположить, что их основная степень окисления должна равняться 2+. В действительности основная степень окисления лантаноидов равна 3+. Что же касается двухвалентного состояния, то оно хоть и известно для всех лантаноидов, но его устойчивость, особенно в водных растворах, весьма неодинакова для различных представителей этого семейства и определяется величиной стандартного окислительно-восстановительного потенциала Е° (Ln3+/Ln2+). Этот потенциал связан с изменением энергии Гиббса реакции
Ln2+ (aq) + H+ (aq) = Lnз+ (aq)+l/2H2(г) (1)
уравнением
∆Gо = - FEо(Ln3+/Ln2+)
∆Gо реакции (1) может быть найдено с помощью термодинамического цикла:
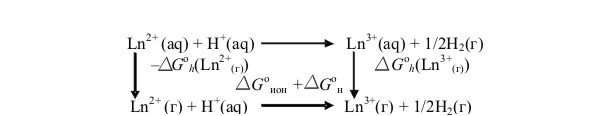
где ∆G°h(Ln2+(г)) и ∆G°(Ln3+(г)) соответственно изменения энергии Гиббса при гидратации ионов Ln2+ и Ln3+; ∆G°ион - изменение энергии Гиббса, соответствующее ионизации двухзарядных ионов с превращением их в трехзарядные; ∆G°н - изменение энергии Гиббса реакции восстановления протонов до газообразного водорода;
H+(aq) + e = l/2H2(г).
Эта последняя величина, по некоторым данным, составляет приблизительно - 458 кДж/моль. Энергии гидратации ионов ∆G° и энергии ионизации ∆G°ион приведены в табл. 33.
Таблица 33
|
Элемент |
∆Gоион, кДж/моль |
-∆Gоh(Ln3+(г)), кДж/моль |
-∆Gоh(Ln3+(г)), кДж/моль |
|
Ce |
1949 |
3192 |
1397 |
|
Pr |
2086 |
3233 |
1309 |
|
Nd |
2132 |
3266 |
1317 |
|
Pm |
2152 |
3297 |
1346 |
|
Sm |
2258 |
3310 |
1341 |
|
Eu |
2404 |
3362 |
1361 |
|
Gd |
1990 |
3379 |
1550 |
|
Tb |
2114 |
3414 |
1463 |
|
Dy |
2200 |
3448 |
1437 |
|
Ho |
2204 |
3469 |
1433 |
|
Er |
2194 |
3489 |
1453 |
|
Tm |
2285 |
3513 |
1451 |
|
Yb |
2417 |
3555 |
1461 |
а) На основании приведенного термодинамического цикла и используя данные табл. 33, вычислите стандартные окислительно-восстановительные потенциалы Е°(Ln3+/Ln2+) лантаноидов. Рассчитанные Вами значения сопоставьте с экспериментальными данными, приведенными в табл. 32. Обратите внимание на то, что при некоторой завышенности рассчитанных значений по сравнению с экспериментальными, общий характер изменения Е°(Ln3+/Ln2+) в зависимости от атомного номера элемента сохраняется.
б) Какие из ионов Ln2+ наиболее устойчивы в водном растворе и какие наименее устойчивы? Для одного из ионов Ln2+, явно неустойчивого в водной среде, напишите уравнение реакций его взаимодействия с водой, составив уравнения полуреакций. Учтите, что стандартный окислительно-восстановительный потенциал восстановительного разложения воды равен - 0,41 В.
в) Как согласуются с известными экспериментальными значениями ° (Ln3+/Ln2+) следующие наблюдения:
1. Все Ln2+ относятся к сильным восстановителям.
2. В водных растворах устойчив лишь Еu2+, водные растворы которого (бесцветные на вид) стабильны в течение более чем 10 дней в отсутствие окислителей.
3. Растворы Yb2+, приготовленные при использовании воды, не содержащей О2, длительное время сохраняются с присущей им светло-зеленой окраской.
4. Растворы Sm2+' менее устойчивы, но характерный для них красный цвет сохраняется несколько часов.
5. Соединения Тm2+ практически мгновенно окисляются водой, давая кратковременное красно-фиолетовое окрашивание.
На основании всех этих экспериментальных наблюдений и соответствующих окислительно-восстановительных потенциалов расположите в ряд в порядке уменьшения их устойчивости в водных растворах те ионы, о которых шла речь выше.
г) Чем, с точки зрения электронной конфигурации ионов Ln2+, объясняется повышенная устойчивость двухвалентного состояния европия и иттербия по сравнению с другими лантаноидами?
3.49. Изобразите термодинамический цикл, соответствующий реакции
LnF4(к) = LnF3(к) + l/2F2(г)
На основании этого цикла:
а) Получите выражение для ΔG0 этой реакции.
б) Какая величина будет определять изменение энергии Гиббса реакции разложения для различных лантаноидов?
в) Согласуется ли Ваш ответ с тем фактом, что температуры разложения СеF4, PrF4 и TbF4 - примерно составляют 1070, 360 и 470 К соответственно и что тетрафториды других лантаноидов неизвестны?
3.50. До настоящего времени проблема размещения f-элементов в Периодической системе остается предметом дискуссий. Выделение лантаноидов и актиноидов в отдельные семейства, вынесенные за пределы Периодической системы, вызывает возражения со стороны многих исследователей, справедливо считающих, что, согласно идее Д.И. Менделеева каждый химический элемент, должен иметь в системе строго определенное место в соответствии с его химическими свойствами, а также, по современным представлениям, в соответствии с особенностями строения его атома.
Важнейшим критерием принадлежности элемента к той или иной группе Периодической системы является число валентных электронов в его атоме. Для элементов главных подгрупп - это сумма s- и р-электронов. Так, щелочные металлы с одним электроном вне заполненных оболочек относятся к подгруппе 1А, щелочноземельные элементы с двумя такими электронами образуют подгруппу IIА, элементы подгруппы бора с тремя электронами (ns2 + nр1, где n - номер периода) - к IIIА и т. д. Номер группы d-элементов определяется суммой валентных электронов (n-l)d+ns: скандий с тремя валентными электронами 3d14s2 относится к группе IIIВ и т. д.
Если исходить из этой закономерности, то для лантаноидов и актиноидов необходимо суммировать не только их внешние электроны (n-l)d и ns, но и электроны, находящиеся на застраивающемся подуровне (n-2)f. Такое суммирование для многих лантаноидов и актиноидов привело бы к слишком большому числу валентных электронов, которых не может быть более восьми, ибо Периодическая система имеет только восемь групп. Например, для диспрозия с распределением валентных электронов 4f106s2 не нашлось бы места в системе.
Для устранения этого противоречия В.К. Григорович предложил исключить из числа валентных электроны наполовину заполненной подоболочки (n - 2)f7. Тогда число валентных электронов, например, у европия [4f7]6s2 оказывается равным двум, и его можно поместить в подгруппу IIс, гадолиний [4f7]5d16s2 окажется в подгруппе IIIc, тербий [4f7]+26s2 - в подгруппе IVc и т. д.
а) На основании изложенных соображений распределите лантаноиды и актйноиды по группам Периодической системы, продолжив заполнение табл. 34.
Таблица 34
|
Периоды |
Группы |
||||||
|
IIc |
IIIc |
IVc |
Vc |
VIc |
VIIc |
VIIIc |
|
|
6 |
Ba 6s2 |
La 5d16s2 |
Сe 4f2s2 |
... |
... |
... |
... |
|
... |
... |
... |
... |
... |
... |
... |
|
б) Обсудите достоинства и недостатки такого распределения.
в) Воспользовавшись справочной, монографической и учебной литературой, сопоставьте свойства элементов по группам, обратите особое внимание на выявленные сходства и различия элементов, попадающих в одну и ту же группу. На основании этого сопоставления сделайте заключение о правомерности, такого подхода к проблеме размещения f-элементов в Периодической системе.
