
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания

ФЕРРИТЫ-ХРОМИТЫ ПЕРЕХОДНЫХ ЭЛЕМЕНТОВ: СИНТЕЗ, СТРУКТУРА, СВОЙСТВА
Иванов В В, Ульянов А К, Шабельская Н П,
2.4. Кинетика образования ферритов-хромитов меди (II)
Согласно проведенному аналитическому обзору, изучению кинетики синтеза твердых растворов состава CuFe2–xCrxO4 в литературе уделено недостаточно внимания. Приводятся сведения по отдельным составам, обычно только ферритам или только хромитам. Межу тем, шпинели рассматриваемой системы находят широкое применение в качестве материалов с ферримагнитными свойствами и в качестве катализаторов.
Для приготовления образцов твердых растворов CuFe2–xCrxO4 были использованы оксиды железа (III), хрома (III) и меди (II) марки хч. Синтезировали образцы аналогично описанному в п. 2.1 при температурах 900, 1000 и 1100 °С. Параметры элементарных ячеек определяли по линии (440) (кубическая фаза), (440) и (404) (тетрагональная фаза со степенью тетрагональности c/a < 1), (400) и (224) (тетрагональная фаза с c/a > 1). На рис. 2.19 приведены рентгенограммы образцов, синтезированных при температуре 1000 °С с параметром состава х = 0; 1,0; 2,0. Анализ рентгенограмм дает следующие результаты: образцы с параметрами состава 0 ? х ? 0,3 и 1,6 ? х ? 2 твердых растворов CuFe2–хCrхO4 имеют структуру тетрагонально-искаженной шпинели. Рентгенограммы составов в указанных интервалах значений х характеризуются заметным расщеплением спектральных линий (рис. 2.19 а, в). В интервале значений 0,3 ? х ? 1,6 образцы имеют структуру кубической шпинели с межплоскостными расстояниями 0,2550, 0,2430, 0,2110 и 0,1620 нм (рис. 2.19).
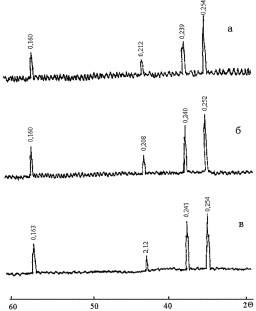
Рис. 2.19. Рентгенограммы образцов твердых растворов CuFe2–xCrxO4:
а – х = 0,0; б – х = 1,0; в – х = 2,0
Для системы CuFe2–хCrхO4 в интервале 0 ? х ? 0,3 образцы твердых растворов представляют собой тетрагонально искаженную структуру шпинели с параметром тетрагональности c/a > 1 (пространственная группа I41/amd), фаза Т2 (рис. 2.20). По мере увеличения значения х степень тетрагональности уменьшается и при х = 0,4 начинается область существования кубических твердых растворов (до х = 1,1 включительно) (пространственная группа Fd3m), фаза К.
В интервале концентраций 1,2 ? х ? 1,8 характер изменения дифракционной картины свидетельствует о наличии двухфазной области. По-видимому, в ней сосуществуют твердые растворы, приблизительно соответствующие составу CuFe0,2Cr1,8O4 (для тетрагональной фазы I41/amd) и CuFe0,8Cr1,2O4 (для кубической фазы). Параметр элементарной ячейки кубической фазы ак твердых растворов практически не меняется, а параметр тетрагональной фазы ст меняется значительно. Это вызывает существенное изменение объема элементарной ячейки тетрагональной фазы (рис. 2.20).
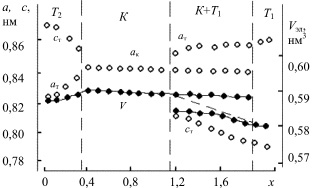
Рис. 2.20. Концентрационные зависимости метрических параметров
и объемов элементарных ячеек фаз шпинелей CuFe2–xCrxO4
В системе CuFe2–xCrxO4 искажения решетки вызываются ян-теллеровскими катионами Cu2+ в А- и В-позициях. В результате кооперативного эффекта ЯТ реализуются два вида низкосимметричных фаз – тетрагональные Т1 и Т2, характеризующиеся удлинением (Т2) и сжатием (Т1) исходной кубической ячейки.
При расчете коэффициента диффузии D использовали формулу (1.2). Результаты расчета приведены в табл. 2.5 и представлены на рис. 2.21. При расчете величины v использовали отношение плотности оксида двухвалентного металла (?CuO = 6,4 г/см3 [168]) к величине рентгеновской плотности ?рент шпинельного твердого раствора по [47].
Таблица 2.5
Данные для расчета коэффициента диффузии
в твердом растворе CuFe2–xCrxO4
|
Значения x |
Относительное увеличение объема продукта v |
T = 1173 K |
T = 1273 K |
Q, |
D0•105, см2/с |
||||
|
?•10–3, с |
D•1010, см2/с |
lgD |
?•10–3, с |
D•1010, см2/с |
lgD |
||||
|
0,0 |
2,128 |
36 |
6,527 |
–9,19 |
18 |
13,053 |
–8,88 |
79,97 |
0,253 |
|
0,2 |
2,143 |
108 |
2,160 |
–9,67 |
36 |
6,481 |
–9,19 |
76,90 |
0,092 |
|
0,4 |
2,149 |
324 |
0,718 |
–10,14 |
108 |
2,154 |
–9,67 |
123,03 |
2,411 |
|
0,6 |
2,159 |
396 |
0,585 |
–10,23 |
144 |
1,608 |
–9,79 |
109,19 |
0,494 |
|
0,8 |
2,168 |
468 |
0,493 |
–10,31 |
180 |
1,281 |
–9,89 |
115,34 |
0,692 |
|
1,0 |
2,178 |
504 |
0,455 |
–10,34 |
180 |
1,275 |
–9,89 |
116,90 |
0,803 |
|
1,2 |
2,179 |
828 |
0,277 |
–10,56 |
288 |
0,797 |
–10,10 |
119,96 |
0,701 |
|
1,4 |
2,196 |
972 |
0,234 |
–10,63 |
360 |
0,632 |
–10,20 |
127,70 |
1,083 |
|
1,6 |
2,200 |
1008 |
0,225 |
–10,65 |
360 |
0,631 |
–10,20 |
130,25 |
1,396 |
|
1,8 |
2,205 |
972 |
0,233 |
–10,63 |
360 |
0,630 |
10,20 |
127,97 |
1,123 |
|
2,0 |
2,199 |
621 |
0,366 |
–10,44 |
216 |
1,053 |
–9,98 |
144,00 |
8,538 |
На концентрационной зависимости энергии активации диффузии (рис. 2.21) можно выделить по крайней мере две области, связанные, по-видимому, с различным механизмом диффузии. По аналогии с результатами, получеными для системы ZnFe2–xCrxO4, V-образное изменение Q(х) можно объяснить следующим образом. Для составов с преобладанием катионов Fe3+ массоперенос осуществляется, вероятно, по типу в, рис. 1.2 за счет взаимной диффузии катионов Cu2+ и Fe3+. В случаях твердых раствором с повышенным содержанием Cr3+ (х > 1,0), происходит смена механизма (массоперенос осуществляется по типу а, рис. 1.2) преимущественно за счет Cu2+.
В области существования тетрагональной фазы I41/amd со степенью тетрагональности c/a > 1 (Т2) (рис. 2.20) при значениях параметра состава 0 ? х < 0,4 отмечено значительное (до 25 %) снижение значений Q и одновременно увеличение коэффициента диффузии D (в 9 раз) (рис. 2.21). Для интервала концентраций 1,2 ? х ? 2,0 (область кристаллизации тетрагональной фазы Т1), напротив, отмечено увеличение значений Q (до 11 %), а рост значений D (в 1,6 раза) меньше, чем можно было бы предположить, анализируя зависимости D(х) для других изученных систем. Таким образом, аналогично системе твердых растворов NiFe2–xCrxO4, можно отметить, что при образовании фазы Т1 возникают кинетические затруднения формирования структуры, при образовании фазы Т2 процесс проходит легче.
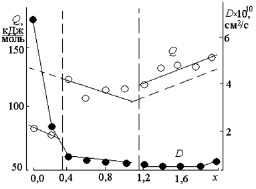
Рис. 2.21. Концентрационные зависимости энергии активации диффузии (Q) и коэффициента диффузии (D) при температуре синтеза 900 °С твердых растворов CuFe2–xCrxO4
Для изучаемой системы рассчитанные значения температурного коэффициента скорости реакции составляют ? = 1,072–1,116.