
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
МЕТОДЫ ФОТОМЕТРИЧЕСКОГО АНАЛИЗА В САНИТАРНО-ГИГИЕНИЧЕСКИХ ИССЛЕДОВАНИЯХ
Дорогова В Б, Игнатьева Л П,
6.4. Определение экстракционно-фотометрическим методом
Работа 4. Определение никеля в присутствии кадмия, марганца и цинка с помощью 1-(2-пиридилазо)-2-нафтола
Пиридилазонафтолаты никеля, кадмия, марганца и цинка имеют следующие экстракционные и фотометрические характеристики:
|
Экстрагируемый комплекс |
?макс, нм |
?мaкс-10-4 |
pH? |
lgKэкс |
|
NiR2 |
575 |
5,1 |
2,1 |
1,9 |
|
CdR2 |
560 |
4,9 |
7,0 |
-7,9 |
|
MnR2 |
550 |
5,9 |
8,5 |
-11,0 |
|
ZnR2 |
560 |
2,9 |
5,7 |
-5,3 |
Оптимальное значение рН для экстракции пиридилазонафтолата никеля находится в интервале 4,0–8,0. Условия экстракционного разделения и селективного экстракционно-фотометрического определения Ni выполняются при pН = 4,0–6,0 – для Cd, 4,0 – для Zn и 4,0–г–7,0 –
для Мn. Поэтому ионы никеля можно определять с помощью ПАН в присутствии соизмеримых количеств Cd, Mn и Zn, экстрагируя хелатный комплекс NiR2 хлороформом при рН ? 4,0. При этом отпадает необходимость предварительного отделения или маскирования Cd, Mn и Zn.
Реактивы
Стандартные растворы нитратов никеля, кадмия, марганца и цинка, содержащие 2–4 мкг Ni, Cd, Mn и Zn в 1 мл.
KNО3, х. ч., 1 М раствор.
ПАН, 0,01 М спиртовый раствор.
Аммиак, 10 % раствор.
Хлороформ, ч. д. а.
Выполнение работы
К кислому раствору, содержащему до 20 мкг никеля, кадмия, марганца и цинка, добавляют 1 мл 1 М раствора KNО3, 1 мл. 0,01 М спиртового раствора реагента ПАН и доводят объем дистиллированной водой до 10 мл. Через 5 мин к раствору с выпавшим осадком добавляют 10 мл хлороформа и встряхивают смесь на механическом встряхивателе колб в течение 5 мин. После расслаивания органическую фазу фильтруют через комочек сухой ваты в кювету с толщиной слоя 1 см, и измеряют оптическую плотность раствора при 575 нм относительно экстракта холостого опыта. Исходное значение рН (~4,5) создают добавлением растворов NH3 и HNO3. Значение рН водных растворов после экстракции контролируют с помощью рН-метра, обеспечивая их равновесные значения в интервале 4,0–4,5. Содержание никеля находят по градуировочному графику.
Результаты определения 11,7 мкг Ni в присутствии 11,0 мкг Cd, 11,0 мкг Мn и 13,0 мкг Zn характеризуются высокой воспроизводимостью (при п = 5, Р = 0,95; s, = 0,024; тNi = 11,7 ± 0,3 мкг).
Работа 5. Определение йода в воде (МУК 4.1.747-99)
Измерение концентрации йода основано на окислении йодида в кислой среде азотистой кислотой до свободного йода, извлечении его из воды четыреххлористым углеродом и последующем фотометрировании окрашенных растворов.
Реактивы:
Вода дистиллированная ГОСТ 6709–72,
Калий йодистый, х.ч. ГОСТ 4232–74,
Кислота серная, х.ч. ГОСТ 4204–77,
Четыреххлористый углерод, х.ч. ГОСТ 20228–74,
Натрий азотистокислый, х.ч., ГОСТ 4197–74.
Исходный раствор йодида в воде (с = 0,1 мг/см3), 0,1308 г калия йодистого вносят в мерную колбу, вместимостью 1 дм3, доводят дистиллированной водой до метки и тщательно перемешивают.
Кислота серная (1:1). К 50 см3 дистиллированной воды осторожно приливают 50 см3 концентрированной серной кислоты.
Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость оптической плотности раствора от массы йода в анализируемой пробе, устанавливают по 5-и сериям растворов для градуировки. Каждую серию, состоящую из 6-и растворов, готовят из свежеприготовленного исходного раствора калия йодистого. Для этого в мерные колбы, вместимостью 500 см3, помещают исходные растворы в соответствии с таблицей, доводят объем до метки дистиллированной водой и тщательно перемешивают.
Таблица 6.1
Растворы для установления градуировочной характеристики
при определении концентрации йода
|
Номер раствора для градуировки |
1 |
2 |
3 |
4 |
5 |
6 |
|
Объем исходного раствора йода (с = 0,1 мг/см3), см3 |
0,5 |
1,0 |
1,5 |
2,5 |
5,0 |
10,0 |
|
Концентрация йода в растворе, мг/дм3 |
0,1 |
0,2 |
0,3 |
0,5 |
1,0 |
2,0 |
Каждый раствор для градуировки и переносят в делительную воронку, добавляют 5 см3 раствора серной кислоты и на кончике пинцета кристаллический натрий азотистокислый. Смесь перемешивают и оставляют стоять 10 минут. Одновременно готовят холостой раствор, в который добавляют те же реактивы, за исключением раствора йода. Через 10 минут во все растворы приливают 10 см3 четыреххлористого углерода и в течение 5 минут проводят экстракцию йода. После разделения слоев четырехслоистый углерод сливают в пробирки с притертыми пробками для анализа, водный верхний слой отбрасывают.
Оптическую плотность растворов измеряют при длине волны 520 нм. по отношению к холостому раствору в кюветах шириной 10 мм.
Градуировочную характеристику устанавливают по средним значениям оптической плотности растворов для градуировки.
Выполнение измерений:
500 см3 анализируемой пробы воды помещают делительную воронку, добавляют реактивы и анализируют аналогично растворам для градуировки.
Концентрацию йода в воде (с) определяют по градуировочной характеристике (мг/см3).
Вычисляют среднее значение концентрации йода в воде их 2-х параллельных определений.
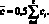
Рассчитывают относительную разницу 2-х параллельных измерений одной пробы:
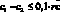
где r – оперативный контроль повторяемости, равный 25,9 %.
Оперативный контроль погрешности
Образцами для контроля являются реальные пробы питьевой воды, к которым делаются добавки измеряемых веществ в виде раствора. Отбирают 2 пробы воды и к одной из них делают добавку таким образом, чтобы содержание определяемого йода увеличилось по сравнению с другой пробой на 50–150 %. Каждую пробу анализируют в точном соответствии с прописью методики и получают результат анализа исходной рабочей пробы (сисх) и рабочей пробы с добавкой (c).
Результаты контроля признаются удовлетворительными, если выполняется условие:
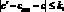
где с – добавка вещества, мг/см3; k – норматив оперативного контроля погрешности, мг/см3.
При внутрилабораторном контроле (Р = 0,90) принимают:
Ќ = 0,84k;
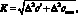
где ?c и ? сисх – характеристики погрешности для исходной пробы и пробы с добавкой, мг/см3
?сисх = 0,01•?отн•сисх;
?c = 0,01•?отн c.