
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания

ПАРАТГОРМОН-РОДСТВЕННЫЙ ПРОТЕИН
Курзанов А. Н., Ледванов М. Ю., Быков И. М., Медведев В. Л., Стрыгина Е. А., Бизенкова М. Н., Заболотских Н. В., Ковалев Д. В., Стукова Н. Ю.,
3.3.1. Участие паратгормон-родственного белка в регуляции клеточной пролиферации и дифференцировки
ПТГрП участвует в модуляции выживаемости клеток, пролиферации, апоптоза и морфогенетической дифференцировки (Karaplis A.C., 2001; Lanske B., Kronenberg H.M., 1998; Luparello C., 2011; Martin T.J. et al., 1997; Wysolmerski J.J., 2012). Множественность действий ПТГрП в этих разнообразных клеточных реакциях зависит от его способности действовать как паракринный и аутокринный фактор (Clemens T.L. et al., 2001; Philbrick W.M. et al., 1996). Эта универсальность позволяет ПТГрП действовать как ключевой фактор развития, который может регулировать дифференциацию и рост нескольких тканей и органов (Clemens T.L. et al., 2001; Karperien M. et al., 1996; Martin T.J. et al., 1997; Philbrick W.M. et al., 1996, Wysolmerski J.J., Stewart A.F., 1998). Сообщалось о влиянии ПТГрП, а также его биологически активных фрагментов на пролиферацию, или, наоборот, гибель клеток в модельных системах нормальных тканей (Chen H.L. et al., 2002; Hastings R.H. et al., 2003; Alonso V. et al., 2008).
ПТГрП участвует в регуляции роста и дифференцировки многих типов клеток: костной ткани и почек, АПУД системы, молочной железы, легких, мозга, сердца, сосудов и других. Влияние этого белка на рост и дифференцировку клеток в различных нормальных тканях начинается с самых ранних этапов эмбриогенеза. В исследованиях in vitro и in vivo установлено, что ПТГрП может изменять рост и дифференцировку кератиноцитов (Kaiser S.M. et al., 1992), клеток мозга (Macica C.M., Broadus A.E., 2003), клеток молочных желез (Van Houten J.N. et al., 2003), респираторных эпителиоцитов (Hastings R.H. et al., 2003), почечных клеток (Aya K. et al., 1999), гладкомышечных клеток (Stuart W.D. et al., 2000), β-клеток поджелудочной железы (Cebrian A. et al., 2002), клеток хрящевой эпифизарной пластины (Amizuka N. et al., 1994).
Считается, что ПТГрП принадлежит ключевая роль в контроле темпов созревания хондроцитов в хрящевой ростовой пластине посредством предотвращения преждевременной дифференциации хондроцитов в прегипертрофированные и в гипертрофированные хондроциты (Lanske B. et al., 1999), а также путем увеличения скорости пролиферации хондроцитов и подавления их терминальной дифференцировки. Эти эффекты возникают из-за взаимодействия ПТГрП с рецептором ПТГ/ПТГрП (рис. 9).
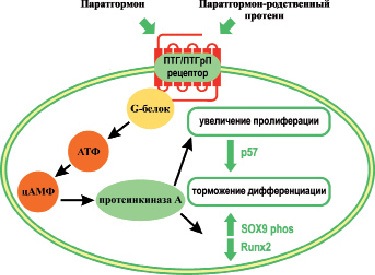
Рис. 9. Активация рецептора ПТГ/ПТГрП приводит к активации нескольких G-белков. Активация белка Gs приводит к последующей активации аденилатциклазы и генерации циклического АМФ. Циклический АМФ имеет несколько действий, включая активацию протеинкиназы A, что приводит к уменьшению уровней белка p57, ингибирующего активность циклин-зависимой киназы и белка Runx2, являющегося фактором транскрипции, который необходим для гипертрофической дифференцировки хондроцитов в большинстве костей. Снижение уровня p57 приводит к увеличению пролиферации и торможению дифференцировки хондроцитов. Ингибирование производства Runx2 под влиянием ПТГрП, способствует задержке дифференциации хондроцитов. РКА также фосфорилирует фактор транскрипции SOX9, действующий во время дифференцировки хондроцитов
Ингибирование воздействия ПТГрП на хондроциты путем прерывания сигнализации через ПТГ/ПТГрП-рецепторы приводит к ускорению дифференцировки хондроцитов и преждевременному исчезновению пластины роста (Hirai T. et al., 2011; Horwitz M.J. et al., 2010).