Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
§ 2.1.9. Кислородсодержащие органические соединения
Органические вещества, молекулы которых включают, помимо углерода и водорода другие элементы периодической системы называют производными углеводородов.
Производные углеводородов, содержащие в своих молекулах кислород, называют кислородсодержащими органическими соединениями. Представителями кислородсодержащих органических соединений являются: спирты, альдегиды, кетоны, карбоновые кислоты и некоторые другие вещества.
Спиртами называются производные углеводородов, в молекулах которых один или несколько атомов водорода замещены функциональными гидроксогруппами. Если гидроксогруппой замещён один атом водорода, то спирт называется одноатомным, если два и более атомов водорода, то многоатомным. Например:
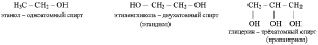
Важно подчеркнуть, что при одном и том же атоме углерода не может находиться более одной гидроксогруппы.
Систематические названия спиртов производятся добавлением суффикса -ол к названию соответствующего углеводорода и при необходимости указанием номера атома углерода, при котором находится группа –ОН:
СН3–СОН–СН3.
пропанол-2
Спирты, в отличие от неорганических оснований, при растворении в воде не диссоциируют и не образуют аниона ОН–.
Альдегидами называются производные углеводородов, содержащие альдегидную функциональную группу:
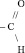
например,
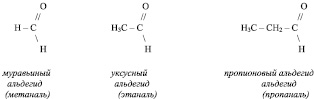
Систематические названия альдегидов производятся добавлением суффикса – аль к названию соответствующего углеводорода.
Кетонами называются производные углеводородов, содержащие карбонильную группу
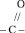
соединённую с двумя углеводородными радикалами. Например,
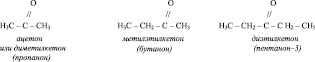
Систематические названия кетонов производятся добавлением суффикса -он к названию соответствующего углеводорода и при необходимости указанием номера атома углерода, при котором находится карбонильная группа.
Карбоновыми кислотами называются производные углеводородов, содержащие карбоксильную функциональную группу:
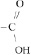
например:
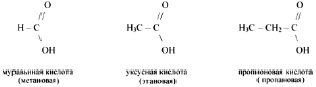
Следует подчеркнуть, что фрагмент
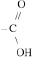
рассматривается в органической химии в качестве единой функциональной карбоксильной группы, хотя формально состоит из двух групп – карбонильной и гидроксогруппы.
Карбоновые кислоты, включающие в свой состав кратные углерод-углеродные связи называются непредельными кислотами[27], например:
СН2=СН–СООН СН2=СН–СH2–СООН СН3–СН=СН–СООН
акриловая кислота винилуксусная кислота кротоновая кислота
(пропеновая) (бутен-3-овая) (бутен-2-овая)
Непредельные кислоты относятся к органическим соединениям со смешанными функциями, то есть, включающими различные функциональные группы.
Систематические названия карбоновых кислот производятся добавлением окончания -овая к названию соответствующего углеводорода и слова «кислота».
Карбоновые кислоты, подобно неорганическим кислотам, при растворении в воде диссоциируют, отщепляя катион Н+:
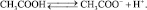
Физические свойства
Даже низшие спирты – метанол и этанол являются жидкостями при нормальных условиях, в то время как соответствующие углеводороды представляют собой газы. Низшие альдегиды, кетоны и кислоты также являются жидкостями за исключением метаналя, который кипит при –21 °С. Такое агрегатное состояние кислородсодержащих органических соединений объясняется наличием водородных связей[28] между молекулами веществ, объединяющих эти молекулы в одно единое целое.
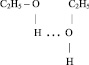
Хотя водородные связи намного слабее ионных и ковалентных связей, однако, их прочность достаточна для того, чтобы существенно влиять на агрегатное состояние веществ.
Химические свойства
Реакции соединения. Присоединение к органической молекуле возможно только в том случае, если она содержит двойную или тройную связь, включающую в себя непрочную, легко разрывающуюся π-связь.
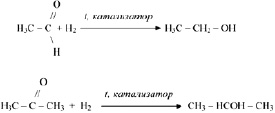
Аналогично присоединяют водород и другие альдегиды и кетоны. Однако, для карбоновых кислот реакции присоединения водорода не характерны.
Кроме того, альдегиды способны соединяться со спиртами, образуя полуацетали:
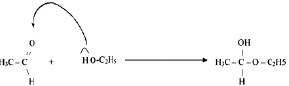 (2.20)
(2.20)
этилполуацеталь этаналя
Реакции разложения. При нагревании до температуры 140 °С и в присутствии концентрированной серной кислоты многие одноатомные спирты образуют алкены, отщепляя воду (реакция дегидратации):
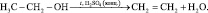
Метанол в результате отщепления водорода (реакция дегидрирования) может образовать метаналь

Муравьиная кислота при нагревании и в присутствии концентрированной серной кислоты разлагается на воду и угарный газ
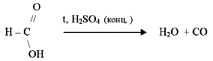
Реакции замещения. Подобно воде спирты реагируют с активными металлами

этилат натрия
Благодаря наличию углеводородного радикала кислородсодержащие органические соединения могут вступать в реакции замещения с галогенами подобно алканам:
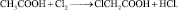
хлоруксусная кислота
Реакции обмена. Спирты взаимодействуют с кислотми.
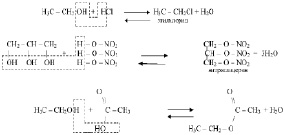 (2.21)
(2.21)
Обратите внимание, что механизм взаимодействия спиртов с карбоновой кислотой существенно отличается от механизма взаимодействия с неорганическими кислотами. Для образования воды карбоновая кислота предоставляет гидроксогруппу, в то время как неорганические кислоты предоставляют атомы водорода.
Реакции взаимодействия спиртов с карбоновыми кислотами называются реакциями этерификации (от лат. ester – эфир). Органические продукты реакции этерификации называются сложными эфирами.
Сложные эфиры, образованные в результате этерификации глицерина и карбоновых кислот называются жирами:
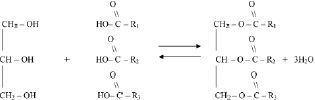
где R1 R2 R3 – различные углеводородные радикалы – насыщенные и ненасыщенные.
Процесс, обратный этерификации глицерина, называется гидролизом жиров. Природные жиры[29], входящие в состав клеток растений и животных включают R1, R2 и R3, содержащие от 3 до 25 атомов углерода. При гидролизе твёрдых природных жиров образуются только предельные карбоновые кислоты, наиболее распространёнными из которых являются пальмитиновая и стеариновая:

Кислоты с такими длинными углеводородными радикалами иногда относят к высшим жирным кислотам[30].
При гидролизе жидких (преимущественно растительных) природных жиров образуются главным образом непредельные карбоновые кислоты, наиболее распространёнными из которых являются олеиновая, линолевая и линоленовая кислоты:
С17Н33СООН С17Н31СООН С17Н29СООН
олеиновая кислота линолевая кислота линоленовая кислота
молекулы спирта могут взаимодействовать и друг с другом
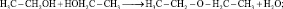 (2.22)
(2.22)
диэтиловый эфир
 (2.23)
(2.23)
метилэтиловый эфир
Органические продукты взаимодействия молекул спирта друг с другом называются простыми эфирами.
Причём, дегидратация спирта, протекающая с образованием простого эфира проводится в аналогичных условиях, что и дегидратация спирта, протекающая с образованием алкена, но при меньшей температуре и большей концентрации спирта.
Взаимодействие альдегидов с аммиачным раствором оксида серебра до сих пор считается классической качественной реакцией, доказывающей наличие группы
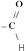
в молекуле вещества. Реакция очень эффектна, так как выделяющееся в результате серебро покрывает стенки реакционной пробирки, делая её поверхность зеркальной, отчего сам процесс называют реакцией «серебряного зеркала». Проводят его в две стадии:
1. Растворяют оксид серебра в водном растворе аммиака

2. К полученному раствору добавляют альдегид и нагревают:
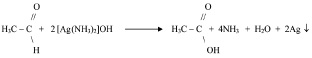
Если уравнения обеих стадий сложить, то суммарная схема процесса окажется следующей:
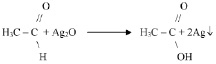
Однако, следует иметь в виду, что в реакцию «серебряного зеркала» вступает и метановая кислота,

К кислородсодержащим органическим соединениям со смешанными функциями, помимо непредельных кислот, относятся также углеводы – вещества, химический состав которых может быть представлен формулой Cn(H2O)m, например:
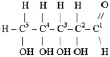
рибоза С5Н10О5 (C5(H2O)5)
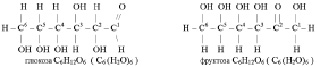
Однако, известно, что альдегиды способны вступать в реакцию присоединения со спиртами (см. реакцию (2.20)). Поскольку в приведённых примерах альдегидная группа и гидроксогруппа находятся при одной молекуле, то они могут соединяться, образуя замкнутый цикл. В водных растворах рибозы альдегидная группа соединяется с гидроксогруппой четвёртого атома углерода. В водных растворах глюкозы с гидроксогруппой пятого атома углерода. В водных растворах фруктозы может происходить соединение карбонильной группы с шестым атомом углерода или с пятым. То есть, в этих условиях существуют обе формы молекул углеводов – циклическая и ациклическая. Но равновесие между ними смещено, всё-таки, в сторону циклических форм. Углеводы, циклическая форма молекул которых представляет собой один цикл, называются моносахаридами.
Подобно спиртам циклические формы молекул углеводов могут вступать в реакцию обмена между собой (см. реакции (2.22) и (2.23)), образуя углеводы с большей молекулярной массой. Например:
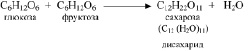
Более того, поскольку углеводы содержат несколько гидроксогрупп, то они способны соединяться друг с другом многократно, образуя макромолекулы с огромной молекулярной массой. Например,
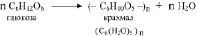
или (при других условиях процесса)
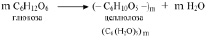
Таким образом, крахмал и целлюлоза представляют собой полимеры (полисахариды), мономером которых является глюкоза. Но целлюлоза отличается значительно бόльшим значением молекулярной массы (m >> n) и отсутствием разветвлений в цепи, характерных для молекул крахмала. Очень близок к крахмалу гликоген (животный крахмал), который откладывается в печени и является резервным веществом в организме человека и животных. Но молекулы гликогена значительно крупнее молекул крахмала и имеют ещё более разветвлённую структуру.
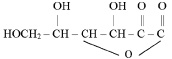
Некоторые витамины – жизненно важные компоненты живых организмов – также относятся к кислородсодержащим соединениям со смешанными функциями. В частности, витамин С (аскорбиновая кислота) представляет собой циклический эфир, содержащий карбонильную и гидроксогруппы:
1. Дайте систематические названия следующим соединениям:
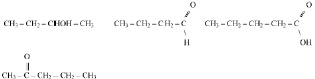
2. Охарактеризуйте химические свойства кислородсодержащих органических соединений, не являющихся углеводами. Что такое жиры? В чём состоит основное отличие химического состава жидких жиров от твёрдых жиров. Опишите реакцию серебряного зеркала.
3. Дайте определения следующим понятиям: углеводы, моносахариды, полисахариды. Приведите примеры этих веществ. Опишите разницу в строении молекул целлюлозы, крахмала и гликогена.
4. Пользуясь равенствами (2.6) и (2.7) расставьте коэффициенты в схеме реакции: