
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
4.2. Плазменно-гидродинамическая концепция состояния ионов в растворах электролитов и определение электропроводности
Исходные предпосылки те же, т.е. два эквивалентных представления плотности тока
![]() , (4.1)
, (4.1)
где ![]() – плотность зарядов;
– плотность зарядов; ![]() – плотность числа ионов в 1 см3 раствора, обеспечивающих удельную проводимость
– плотность числа ионов в 1 см3 раствора, обеспечивающих удельную проводимость ![]() ;
; ![]() – напряженность внешнего поля, под действием которой ионы приобретают направленное движение со скоростью
– напряженность внешнего поля, под действием которой ионы приобретают направленное движение со скоростью ![]() .
.
Отсюда следует ![]() . Эта величина связана с молярной (или эквивалентной) проводимостью
. Эта величина связана с молярной (или эквивалентной) проводимостью ![]() следующим стандартным выражением при молярной концентрации эквивалента электролита
следующим стандартным выражением при молярной концентрации эквивалента электролита ![]() в виде
в виде ![]() . Учитывая здесь предыдущее выражение для
. Учитывая здесь предыдущее выражение для ![]() , можно получить:
, можно получить:
![]() .
.
Согласно [105], плотность числа ионов ![]() равна:
равна:
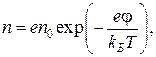
и равновесная плотность числа ионов ![]() в 1 см3 раствора связана с молярной концентрацией эквивалента электролита
в 1 см3 раствора связана с молярной концентрацией эквивалента электролита ![]() следующим известным соотношением
следующим известным соотношением ![]() . Тогда
. Тогда
![]() ,
,
где ![]() – число Фарадея;
– число Фарадея; ![]() – число Авогадро. Если умножить и разделить правую часть на величину элементарного заряда
– число Авогадро. Если умножить и разделить правую часть на величину элементарного заряда ![]() :
:
![]() , (4.17)
, (4.17)
то появляется возможность связать скорость движения зарядов ![]() с силой внешнего электрического поля
с силой внешнего электрического поля ![]() и с силой сопротивления в виде силы вязкости среды
и с силой сопротивления в виде силы вязкости среды ![]() посредством уравнения движения:
посредством уравнения движения:
![]() .
.
Здесь ![]() – сила сопротивления, и потому имеет знак (–).
– сила сопротивления, и потому имеет знак (–).
В условиях стационарного тока в растворе, средняя скорость ![]() , имеет место
, имеет место ![]() . Тогда выражение (4.17) приводится к виду [106]:
. Тогда выражение (4.17) приводится к виду [106]:
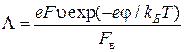 ,
,
где значение силы вязкости ![]() определяется уравнением (3.42):
определяется уравнением (3.42): 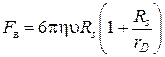 , в котором
, в котором ![]() – динамическая вязкость в пуаз (пуаз = г×сек–1см–1),
– динамическая вязкость в пуаз (пуаз = г×сек–1см–1), ![]() – приведенный радиус гидратированных ионов, рассчитываемый по уравнению:
– приведенный радиус гидратированных ионов, рассчитываемый по уравнению:
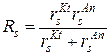 , (4.18),
, (4.18),
где ![]() и
и ![]() – радиусы гидратированных ионов, определяемые уравнением (3.9);
– радиусы гидратированных ионов, определяемые уравнением (3.9); ![]() – дебаевский радиус экранирования зарядов (
– дебаевский радиус экранирования зарядов (![]() – диэлектрическая постоянная растворителя, например, для воды
– диэлектрическая постоянная растворителя, например, для воды ![]() = 78 при 25 °С).
= 78 при 25 °С).
Таким образом, молярная электропроводность эквивалента электролита приобретает следующий вид:
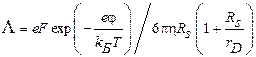 . (4.19)
. (4.19)
Учитывая в уравнении (4.19) значение выражения (3.7) для определения потенциальной энергии и значение числа Фарадея в виде ![]() , получим уравнение для расчета электропроводности [108-110]:
, получим уравнение для расчета электропроводности [108-110]:
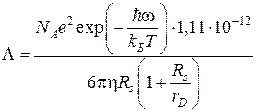 , Ом-1см2моль-1. (4.20)
, Ом-1см2моль-1. (4.20)
где согласно [107] в системе СГС значение 1 Ом = 1,11×10-12 см-1×сек. При подстановке всех постоянных уравнение (4.20) имеет вид:
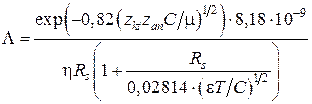 .
.
Справедливость приведенных рассуждений и уравнения (4.20) можно показать на примерах расчетов ![]() для I-I, I-II и II-I электролитов.
для I-I, I-II и II-I электролитов.
Результаты теоретических оценок эквивалентных электрических проводимостей растворов электролитов в рамках плазменно-гидродинамической модели приведены в табл. 4.1–4.11 и на рис. 1,2. Литературные значения ![]() взяты из [111].
взяты из [111].
Таблица 4.1
Эквивалентная электропроводность (![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() в зависимости от концентрации при 298 K
в зависимости от концентрации при 298 K ![]() = 13,92;
= 13,92; ![]() = 1,75×10-8 см;
= 1,75×10-8 см; ![]() = 1,34×10-8 см;
= 1,34×10-8 см; ![]() = 0,76×10-8 см
= 0,76×10-8 см
|
|
0 |
0,1 |
0,5 |
2 |
4 |
5 |
|
|
0 |
0,083 |
0,190 |
0,378 |
0,535 |
0,600 |
|
|
1,000 |
0,930 |
0,850 |
0,730 |
0,640 |
0,610 |
|
|
∞ |
13,510 |
6,068 |
3,034 |
2,145 |
1,915 |
|
|
121 |
107 |
92 |
71 |
58 |
53 |
|
|
124 |
106 |
93 |
75 |
57 |
49 |
Таблица 4.2
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 8,96;
= 8,96; ![]() = 3,25×10-8 см;
= 3,25×10-8 см; ![]() = 1,34×10-8 см;
= 1,34×10-8 см; ![]() = 0,73×10-8 см
= 0,73×10-8 см
|
|
0 |
0,005 |
0,025 |
0,25 |
1 |
2,5 |
|
|
0 |
0,047 |
0,105 |
0,334 |
0,668 |
1,056 |
|
|
1,000 |
0,962 |
0,917 |
0,760 |
0,578 |
0,421 |
|
|
∞ |
60,670 |
27,151 |
8,580 |
4,292 |
2,715 |
|
|
126 |
119 |
113 |
88,27 |
62,25 |
30,5 |
|
|
129 |
114 |
103 |
83 |
59 |
32 |
Таблица 4.3
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 12,30;
= 12,30; ![]() = 2,88×10-8 см;
= 2,88×10-8 см; ![]() = 1,34×10-8 см;
= 1,34×10-8 см; ![]() = 0,69×10-8 см
= 0,69×10-8 см
|
|
0,001 |
0,005 |
0,01 |
2 |
3 |
4 |
|
|
0,013 |
0,028 |
4,298 |
0,570 |
0,698 |
0,806 |
|
|
0,989 |
0,977 |
0,967 |
0,626 |
0,564 |
0,516 |
|
|
1,359 |
6,079 |
4,298 |
3,039 |
2,482 |
2,149 |
|
|
130,42 |
127,94 |
126,12 |
67,57 |
58,39 |
51,70 |
|
|
130,31 |
124,25 |
120,36 |
66,65 |
56,6 |
48,35 |
Таблица 4.4
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 7,16;
= 7,16; ![]() = 4,68×10-8 см;
= 4,68×10-8 см; ![]() = 1,34×10-8 см;
= 1,34×10-8 см; ![]() = 0,72×10-8 см
= 0,72×10-8 см
|
|
0,01 |
1 |
2 |
4 |
|
|
0,065 |
0,647 |
0,915 |
1,295 |
|
|
0,948 |
0,588 |
0,472 |
0,346 |
|
|
4,298 |
4,298 |
3,039 |
2,149 |
|
|
118,8 |
64,2 |
48,6 |
32,9 |
|
|
106,9 |
56,2 |
43,7 |
26,4 |
Таблица 4.5
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 41,3;
= 41,3; ![]() = 1,42×10-8 см;
= 1,42×10-8 см; ![]() = 1,23×10-8 см;
= 1,23×10-8 см; ![]() = 0,66×10-8 см
= 0,66×10-8 см
|
|
0,1 |
0,6 |
1,5 |
2,5 |
|
|
0,049 |
0,122 |
0,191 |
0,247 |
|
|
0,961 |
0,904 |
0,855 |
0,817 |
|
|
1,373 |
5,466 |
3,508 |
2,707 |
|
|
127,6 |
112,3 |
100,2 |
91,4 |
|
|
136 |
121 |
116 |
107 |
Таблица 4.6
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 51,08;
= 51,08; ![]() = 1,42×10-8 см;
= 1,42×10-8 см; ![]() = 1,23×10-8 см;
= 1,23×10-8 см; ![]() = 0,66×10-8 см
= 0,66×10-8 см
|
|
0,01 |
0,5 |
1 |
2 |
3 |
5 |
|
|
0,043 |
0,091 |
0,142 |
0,199 |
0,245 |
0,308 |
|
|
0,965 |
0,924 |
0,890 |
0,848 |
0,818 |
0,777 |
|
|
1,380 |
6,269 |
4,246 |
3,009 |
2,457 |
1,952 |
|
|
132,6 |
120,7 |
111,3 |
100,7 |
93,4 |
84,2 |
|
|
137 |
126,5 |
121 |
115 |
106,5 |
87,6 |
Таблица 4.7
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 291K
при 291K ![]() = 9,24;
= 9,24; ![]() = 0,26×10-8см;
= 0,26×10-8см; ![]() = 1,34×10-8см;
= 1,34×10-8см; ![]() = 0,22×10-8см
= 0,22×10-8см
|
|
0 |
0,001 |
0,01 |
0,1 |
5 |
|
|
0,000 |
0,010 |
0,033 |
0,104 |
0,736 |
|
|
1,000 |
0,991 |
0,973 |
0,916 |
0,539 |
|
|
∞ |
48,50 |
15,34 |
48,50 |
6,85 |
|
|
372 |
367 |
361 |
340 |
146 |
|
|
378 |
377 |
370 |
351 |
150 |
Таблица 4.8
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 291K
при 291K ![]() = 9,75;
= 9,75; ![]() = 1,75×10-8 см;
= 1,75×10-8 см; ![]() = 0,43×10-8см;
= 0,43×10-8см; ![]() = 0,345×10-8см
= 0,345×10-8см
|
|
0 |
0,001 |
0,01 |
0,1 |
10 |
|
|
0,000 |
0,010 |
0,32 |
0,319 |
1,011 |
|
|
1,000 |
0,992 |
0,973 |
0,764 |
0,427 |
|
|
∞ |
136,5 |
43,16 |
4,315 |
1,3647 |
|
|
226 |
223 |
216 |
159 |
18,000 |
|
|
220 |
208 |
200 |
160 |
20,0 |
Таблица 4.9
Концентрационная зависимость эквивалентной электропроводности ![]() (
(![]() , Ом-1×см2×моль-1) при 291K
, Ом-1×см2×моль-1) при 291K ![]() = 13,96;
= 13,96; ![]() = 3,13×10-8 см;
= 3,13×10-8 см; ![]() = 1,34×10-8см;
= 1,34×10-8см; ![]() = 0,73×10-8см
= 0,73×10-8см
|
|
0,001 |
0,005 |
0,01 |
0,1 |
0,5 |
1 |
|
|
0,012 |
0,027 |
0,038 |
0,119 |
0,268 |
0,378 |
|
|
0,990 |
0,978 |
0,969 |
0,904 |
0,799 |
0,728 |
|
|
1,365 |
6,103 |
4,316 |
1,365 |
6,103 |
4,316 |
|
|
105,1 |
103,2 |
101,7 |
91,7 |
76,2 |
66,5 |
|
|
107 |
101 |
98 |
82 |
65 |
55 |
Таблица 4.10
Концентрационная зависимость эквивалентной электропроводности ![]() (
(![]() , Ом-1×см2×моль-1) при 291K
, Ом-1×см2×моль-1) при 291K ![]() = 14,76;
= 14,76; ![]() = 2,75×10-8 см;
= 2,75×10-8 см; ![]() = 1,34×10-8см;
= 1,34×10-8см; ![]() = 0,68×10-8см
= 0,68×10-8см
|
|
0,001 |
0,005 |
0,01 |
0,1 |
0,5 |
1 |
|
|
0,012 |
0,026 |
0,037 |
0,116 |
0,260 |
0,368 |
|
|
0,990 |
0,978 |
0,969 |
0,907 |
0,804 |
0,734 |
|
|
1,365 |
6,103 |
4,316 |
1,365 |
6,103 |
4,316 |
|
|
111,9 |
109,9 |
108,5 |
98,1 |
82,1 |
72,0 |
|
|
114,5 |
108,9 |
105,4 |
90,2 |
75,7 |
68,5 |
Таблица 4.11
Концентрационная зависимость эквивалентной электропроводности
(![]() , Ом-1×см2×моль-1)
, Ом-1×см2×моль-1) ![]() при 298K
при 298K ![]() = 3,35;
= 3,35; ![]() = 1,42×10-8 см;
= 1,42×10-8 см; ![]() = 1,23×10-8 см;
= 1,23×10-8 см; ![]() = 0,66×10-8 см
= 0,66×10-8 см
|
|
0,1 |
0,5 |
1 |
3 |
4 |
5 |
|
|
0,244 |
0,546 |
0,773 |
1,338 |
1,545 |
1,728 |
|
|
0,818 |
0,639 |
0,531 |
0,334 |
0,281 |
0,242 |
|
|
1,359 |
6,077 |
4,297 |
2,481 |
2,148 |
1,922 |
|
|
76,529 |
55,397 |
43,637 |
24,303 |
19,684 |
16,370 |
|
|
79,52 |
59,25 |
47,8 |
27,38 |
21,23 |
16,48 |
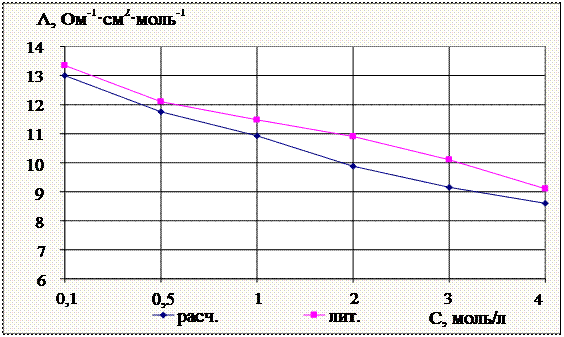

Рис. 1. Графическая зависимость электропроводности ![]() водного раствора
водного раствора ![]() от концентрации при 298K
от концентрации при 298K
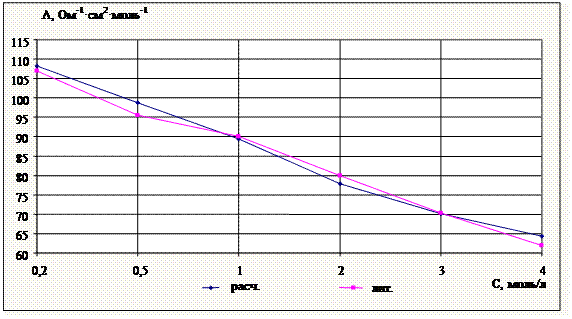

Рис. 2. Графическая зависимость электропроводности ![]() водного раствора
водного раствора ![]() от концентрации при 298K
от концентрации при 298K
