
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
МЕТОДЫ ФОТОМЕТРИЧЕСКОГО АНАЛИЗА В САНИТАРНО-ГИГИЕНИЧЕСКИХ ИССЛЕДОВАНИЯХ
Дорогова В Б, Игнатьева Л П,
3.6. Экстракционно-фотометрический метод
Экстракционно-фотометрический метод основан на сочетании экстракции определяемого вещества и его последующим фотометрировании. Этот метод применяют при анализе сложных смесей, когда нужно определить малые количества одних веществ в присутствии больших количеств других веществ, а также в тех случаях, когда непосредственное определение элемента в смеси связано с большими трудностями.
При экстракции малых количеств примесей происходит не только их выделение, но и концентрирование, Поэтому экстракционно-фотометрический метод приобретает особо важное значение в связи с определением малых количеств примесей в веществах высокой степени чистоты или микропримесей атмосферного воздуха, воздуха рабочей зоны и воды. Экстракционно-фотометрические методы анализа являются высокочувствительного методами и перспективными, особенно для определения металлов, которые образуют разнолигандные
комплексы.
В экстракционно-фотометрических методах для определения металлов применяют экстракционные системы различных типов, выбор которых зависит от химической природы определяемого компонента, состава растворенных веществ и условий проведения экстракции.
Для количественной оценки экстракционного равновесия используют следующие характеристики.
Кд[МRn]/[МRn]-к – константа распределения – отношение концентрации экстрагируемой формы вещества (MRn) в органической фазе к его концентрации в той же самой форме в водной фазе в условиях равновесия. Для каждого несмешивающегося с водой органического растворителя константа распределения является величиной постоянной, при нормальном давлении зависит только от температуры и ионной силы раствора. Если обе жидкие фазы являются насыщенными относительно твердой фазы и равновесие достигнуто, то константа распределения равна отношению растворимостей распределяющегося вещества в органической и водной фазах:
KD = S0/S. (3.20)
Dс = [См]0/[См] – коэффициент распределения[3], (отношение распределения, коэффициент экстракции) – отношение общей аналитической концентрации вещества в органической фазе к его общей аналитической концентрации в водной фазе в условиях равновесия. Поскольку общая аналитическая концентрация является суммой различных ионных форм, соотношение между которыми в водной фазе зависит от рН и концентрации комплексующих реагентов, коэффициент распределения не является постоянной величиной, а зависит от условий эксперимента и константы распределения.
Dm – Qо/Q – массовый коэффициент распределения – отношение количества распределяемого вещества (ммоль) в органической фазе к количеству этого же вещества в водной фазе в условиях равновесия.
Из сопоставления выражений Dc и Dm нетрудно заметить, что
DC = DmW/V и Dm = DcV/W, (3.21)
где V и W – объемы водной и органической фаз.
Если, как это часто бывает при экстракции, V/W = r = 1, то величины Dc и Dm становятся тождественными. При оценке полноты экстракции из выражения массового коэффициента распределения можно найти молярную долю (или процент) вещества, оставшегося в водной фазе после однократной экстракции:
a = (Qисх – Qo)/(Qиcx) = Q/(Qo + Q) = 1/(Dm + 1). (3.22)
При d-кратной экстракции:
a = (1 + Dm)–d. (3.23)
Вычитая из единицы часть вещества, оставшуюся после экстракции (d), получим степень (фактор) извлечения.
Е = Qo/Qиcx = DC/(DC + W/V) = Dm/(1 + Dm). (3.24)
Степень извлечения представляет собой долю или процент от исходного количества вещества в объеме W водной фазы, экстрагируемую объемом V органической фазы при заданных условиях. Если водный раствор обрабатывают d последовательными порциями экстрагента и каждый раз отношение объемов огранической и водной фаз V/W – r, то степень извлечения составляет:
Ed = 1 – (rD + 1)–d. (3.25)
При d = l и r = 1:
E = D/(1 + D). (3.26)
Степень извлечения зависит от тех же факторов, что и коэффициент распределения, и кроме того, от отношения объемов органической и водной фаз.
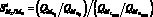 – фактор обогащения – отношение количеств двух разделяемых веществ в фазе экстрагента, отнесенное к исходному отношению их количеств до разделения. Фактор обогащения представляет собою коэффициент, на который нужно умножить исходное отношение количеств двух разделяемых веществ, чтобы получить отношение их количеств в органической фазе после разделения.
– фактор обогащения – отношение количеств двух разделяемых веществ в фазе экстрагента, отнесенное к исходному отношению их количеств до разделения. Фактор обогащения представляет собою коэффициент, на который нужно умножить исходное отношение количеств двух разделяемых веществ, чтобы получить отношение их количеств в органической фазе после разделения.
Следовательно:
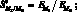 (3.27)
(3.27)
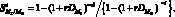 (3.28)
(3.28)
При d = 1 и r = 1:
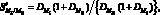 . (3.29)
. (3.29)
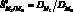 – фактор разделения – отношение коэффициентов распределения двух разделяемых элементов MI и МII.
– фактор разделения – отношение коэффициентов распределения двух разделяемых элементов MI и МII.
Кэкс – константа экстракции – константа равновесия реакции экстракции.
pH1/2 – значение рН раствора, при котором 50 % исходного количества вещества экстрагируется в органическую фазу (D = 1).
Коэффициент распределения является наиболее распространенной характеристикой экстракционных процессов, особенно в условиях конкурирующих равновесий в водной фазе. Эта характеристика, зависящая от условий проведения экстракции и взаимосвязанная с константами распределения и экстракции, позволяет получить объективную количественную информацию в реальных условиях анализа. Во многих случаях коэффициенты распределения определяют экспериментально, однако при определенных условиях их можно прогнозировать и теоретически. Для этого необходимо знать состав экстрагирующихся соединений, их константы распределения и экстракции, а также иметь сведения о конкурирующих реакциях и образующихся соединениях в водном растворе.