
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
4.1. Состояние кровообращения в конечности после переломов
Несмотря на исключительную важность состояния сосудистого русла и микроциркуляции в репаративном костеобразовании, многие аспекты этой проблемы остаются малоизученными. В настоящее время достаточно хорошо установлено, что сохранение магистрального кровотока в передней большеберцовой артерии, а также внутрикостного кровотока (питательная артерия) обеспечивает кровоснабжение костной мозоли.
При травмах происходит значительное повреждение костей и мягких тканей. Функция конечности в процессе лечения восстанавливается при условии улучшения микроциркуляции в области травмы.
Большинство исследований по этой проблеме посвящено оценке регионального и общего кровотока при лечении последствий травмы или при уравнивании длины конечности [112], а микроциркуляция изучена в меньшей мере.
Нами установлено, что у здорового человека через переднюю большеберцовую мышцу протекает 0,053 ± 0,004 мл крови на 1 г ткани в минуту. В то же время известно, что в кортикальном слое диафиза объем кровотока составлял 0,008 ± 0,0006 мл на 1 г кости в минуту, в костном мозге – 0,030 ± 0,002 мл/мин [112].
Под наблюдением находились 68 испытуемых в возрасте
60–75 лет. На 1–2-е сутки после перелома кровообращение в месте перелома было ослаблено. При помощи гамма-камеры отмечалось время поступления меченого пирофосфата в поврежденную конечность (рис. 4.1–4.4). Результаты показали, что с 3-х суток после травмы, по данным с мечеными соединениями, кровообращение начинало ускоряться во всем поврежденном сегменте (208 ± 9,8 %). Величина капиллярного кровотока в передней большеберцовой мышце возрастала до 10,6 ± 0,85 мл (в норме 5,3 ± 0,42 мл). Характер циркуляции крови представлен на рис. 4.1–4.4 Область ускоренной циркуляции была значительно большей, чем место перелома.


27 секунд после инъекции меченого пирофосфата (РФП). Уже заполнены сосуды здоровой конечности (справа). В конечности с переломом (слева) РФП отсутствует
30 секунд после инъекции РФП. Появление меченого пирофосфата (слева) в конечности с переломом
33 секунды после инъекции меченого пирофосфата. Дальнейшее заполнение сосудов (слева) конечности с переломом
36 секунд после инъекции меченого пирофосфата. РФП в травмированной конечности становится больше (слева)
Рис. ٤.١. Разная скорость заполнения РФП сосудистого русла конечности
с переломом (слева) на ٢-е сутки и в здоровой (справа)

Рис. ٤.٢. Заполнение сосудов конечности с переломом (слева) и здоровой конечности (справа) меченым пирофосфатом на ٥٤ с после инъекции
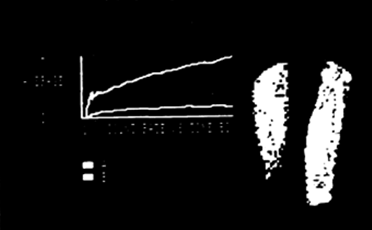
Рис. ٤.٣. Результаты компьютерной обработки данных
о накоплении ٩٩mТс-пирофосфата на ٥٤ с после инъекции:
верхняя кривая – данные в здоровой конечности (справа),
нижняя кривая – данные в травмированной конечности (слева)
В последующие дни (42–46) величина магистрального кровотока возрастала до 240 ± 16,3 %, а капиллярного кровотока – до 12,7 ± 1,01 мл.
Общая закономерность в изменении кровообращения в процессе лечения переломов представлена на рис. 4.5.
Ускорение кровообращения в это время носило локальный характер и соответствовало зоне перелома. На рентгенограммах линия перелома была нечеткой, а количество накапливающегося остеотропного препарата (пирофосфата) возрастало в 7 раз. По линии перелома отмечено небольшое увеличение периостальных напластований.
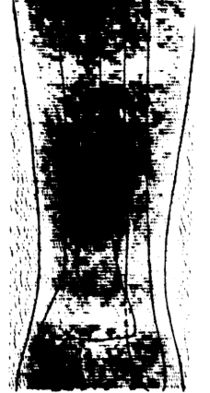

14-й день после перелома 35-й день после перелома
Рис. ٤.٤. Существенное увеличение кровенаполнения сосудистого русла
(по данным с ٩٩mТс-альбумином человеческой сыворотки) в области перелома на ١٤–٣٥ дни
На 6-й неделе начиналось уменьшение объема циркулирующей крови. Величины, близкие к норме (112 ± 4,4 %, что соответствует величине капиллярного кровотока – 5,9 ± 0,4 мл) отмечены на 70-й день. Рентгенологически в зоне периостальных напластований в это время наблюдалось значительное уплотнение, и в большинстве случаев костная мозоль по плотности была равна окружающей ткани. Во всех случаях при этом отмечено утолщение кортикального слоя на 5–15 мм. Одновременно уменьшалась интенсивность обменных процессов, на что указывало существенное ослабление накопления меченого пирофосфата.
На УЗИ первый раз больных обследовали на 3–7-е сутки после травмы и операции наложения аппарата Илизарова. В данный период травматический шок, определяющий состояние сердечно-сосудистой системы, проходил. Второй раз наблюдения были сделаны между 20–30-ми сутками с момента операции. Именно в этот период изменения сердечно-сосудистой деятельности во многом обусловлены особенностями лечения по Илизарову, а не травмой.
42-й день 49-й день 56-й день
Рис. ٤.٥. Изменение интенсивности магистрального
кровотока в месте перелома на ٤٢-٥٦ дни. Данные получены
с ٩٩mТс-альбумином человеческой сыворотки
При расспросе на 3–7-е сутки испытуемые указывали на слабость, сердцебиение, одышку, неопределенные ощущения в области сердца, плохой сон, быструю утомляемость (типичные кардиологические жалобы). В позднем послеоперационном периоде отмечалось улучшение самочувствия. В это время физические нагрузки были в большем объеме: испытуемые активно ходили и занимались лечебной физической культурой. Но при ходьбе довольно часто отмечалось сердцебиение.
После выяснения ощущений и жалоб оценивали ЧСС и АД. В норме минутный объем сердца у здорового взрослого человека в среднем составляет 5,2 литра (по Фику), сердечный индекс в условиях покоя – в среднем 3,75 ± 0,11 л/мин∙м2, а ударный индекс – 49,75 ± 1,75 мл/м2. Сохранение их в пределах нормы обычно свидетельствует об удовлетворительной компенсации интегральной функции сердца. Выход этих показателей за пределы нормы чаще всего указывает на срыв механизмов компенсации. При травме в раннем послеоперационном периоде преобладал гипертензивный
и гиперкинетический тип реакции – у соматически здоровых артериальное систолическое давление повышалось на 20–30 мм рт.ст., диастолическое – на 10–20 мм рт.ст. Типичными были величины 140/90 мм рт.ст., при рабочем давлении 120/80 мм рт.ст. Как правило, наблюдали тахикардию – 90–95 ударов в минуту. На 20–30-е сутки после операции АД и ЧСС приходили к норме (АД – 120/80 мм рт.ст., ЧСС – 68–76 ударов в минуту). Общепериферическое сосудистое сопротивление вначале также чаще было повышено на 10–15 % (N = 1800 дин/с/см) а затем нормализовалось.
Сократимость миокарда левого желудочка ни в первый, ни во второй раз достоверно не отличалась от нормы. Ударный индекс вначале был в пределах нормы, а затем несколько увеличился (в среднем на 5–7 %). Аналогично изменялся и сердечный индекс. Минутный объем кровообращения в раннем послеоперационном периоде составлял 6,75–7,35 литра, затем снижался на 21–23 %, но не доходил до среднефизиологической нормы.
Опираясь на вышесказанное, можно заключить, что в регуляции МОК в позднем послеоперационном периоде у испытуемых преобладает количественный тип приращения деятельности (МОК увеличивается за счет учащения сердечных сокращений и увеличения сердечного и ударного индексов). Такой вариант является энергетически наиболее выгодным.
Оценивая полученные данные, мы пришли к выводу о том, что изменения со стороны сердечно-сосудистой системы у испытуемых в условиях стабильного остеосинтеза носят приспособительный, адаптационный характер.
Для создания оптимальных условий функционирования сердечно-сосудистой системы после травм разрабатывали комплекс фармакологических и организационных мероприятий, а также методик лечебной физической культуры, направленных на нормализацию обнаруживаемых изменений. Такой комплекс позволял улучшить течение репаративного процесса, снизить риск развития осложнений, уменьшить продолжительность лечения и время восстановления трудоспособности.
Таким образом, в области перелома в процессе лечения наблюдалось непрерывное усиление кровообращения, достигавшее наибольших значений на 5-й неделе. В этот же период происходило интенсивное костеобразование, о чем свидетельствовали результаты с меченым пирофосфатом и рентгенологические данные. Тенденция к ослаблению кровотока наблюдалась на 6-й неделе, что свидетельствует о достаточной зрелости регенерата и прочности сращения.
