
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания

Доказательная гипертензиология: количественная оценка результата антигипертензивной терапии.
Николаев Н. А.,
3.3.4. Модельный эксперимент
Основной задачей эксперимента было выявление взаимосвязи приверженности к лечению с количеством и кратностью принимаемых лекарственных средств.
Эксперимент являлся модельным, поскольку в целях соблюдения медицинской и профессиональной этики, в соответствии с Международными этическими правилами для биомедицинских исследований с включением человека CIOMS [9], в эксперименте суррогатно моделировалась ситуация приёма лекарственных средств, при этом участники эксперимента в постоянном приёме каких-либо лекарственных средств на протяжении его проведения не нуждались, а сами средства в используемых дозах значимым терапевтическим и потенциальным нежелательным воздействиями не обладали [8].
В качестве модели лекарственных средств использовали: таблетки аскорбиновой кислоты 0,025 г. (РУПП Белмедпрепараты); таблетки декстрозы моногидрата 0,5 г. (Московская фармацевтическая фабрика). Отбор участников исследования осуществляли из пациентов Городского клинического кардиологического диспансера (г. Омск, Россия) и Регионального центра семейной медицины (г. Омск, Россия). Эксперимент проводился с 15 июня по 1 ноября 2006 года. Последняя дата включения в эксперимент 28 июля 2006 года. В исследование включали добровольцев, подписавших добровольное информированное согласие[1] и соответствующих следующим критериям: гендерный - мужчины (до общего количества 60 человек) и женщины (до общего количества 90 человек) в возрасте от исполнившихся 45 лет, до исполнившихся 74 лет включительно [2]; нозологический - больные ГБ со степенью АГ по данным анамнеза, подтвержденным документально не выше I, I стадии (в соответствии с критериями ESH/ESC 2007) [18], и /или не имеющие других заболеваний, и не нуждающиеся в постоянном приёме антигипертензивных или иных лекарственных средств; социальный - получение заработной платы в качестве основного источника дохода или получение трудовой и/или социальной пенсии; лингвистический - свободное владение устным и письменным русским языком.
Лимитирующими факторами являлись: отсутствие понимания респондентом целей исследования; лекарственная и/или наркотическая и/или токсическая (в т.ч. алкогольная) зависимость, установленная на основании анамнестических данных либо выявленная на любом этапе исследования; возникновение при включении в эксперимент или на этапах эксперимента любых заболеваний, требующих приёма лекарственных средств; прием запрещенных в ходе исследования препаратов[3]; отказ подписать информированное согласие.
Критериями активного прекращения исследования на любом его этапе были определены: решение исследователя, если продолжение участия в эксперименте по какой либо причине оказалось нежелательным для данного добровольца; решение добровольца отказаться от продолжения участия в исследовании.
Используя вышеуказанные критерии, в исследование методом случайной выборки включили 150 добровольцев (стратификация по полу: 60 мужчин и 90 женщин) в возрасте от 46 до 74 лет (средний возраст 52,9 года, медиана 55 лет). Возрастное распределение участников эксперимента отражено в таблице 3.19.
Таблица 3.19
Распределение участников эксперимента по возрастным группам
|
Показатель |
Возраст обследованных, лет |
|||
|
45-49 |
50-59 |
60-69 |
70-75 |
|
|
Участников исследования: |
|
|
|
|
|
всего человек |
28 |
51 |
60 |
9 |
|
% |
18,6 |
34,6 |
40,7 |
6,1 |
|
в том числе: |
|
|
|
|
|
мужчины |
11 |
16 |
27 |
4 |
|
женщины |
17 |
35 |
31 |
5 |
У всех добровольцев был проведён социологический опрос с использованием разработанного автором опросника[4]. После этого методом случайной выборки сформировали 4 группы добровольцев по 37 человек (15 мужчин, 22 женщины) в группе[5].
Каждому добровольцу было поручено в течение 90 дней подряд ежедневно принимать используемые в эксперименте препараты со следующей периодичностью (рис. 10): участникам 1 группы - 1 таблетка препарата «А» 1 раз в сутки 1 раз в сутки (схема 1), участникам 2 группы - 1 таблетка препарата «А» 2 раза в сутки, утром и вечером (схема 2), участникам 3 группы - 1 таблетка препарата «А» 3 раза в сутки, утром, в обед и вечером (схема 3), участникам 4 группы - 2 таблетки препарата «А» и 1 таблетка препарата «В» 1 раз в сутки (схема 4). Все препараты было предписано принимать не разжёвывая, запивая ½ стакана воды.
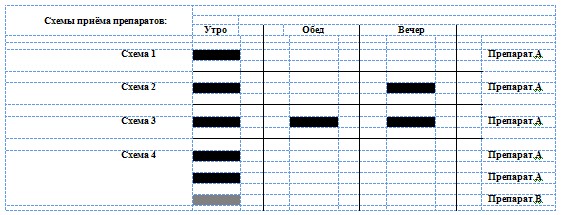
Рисунок 10. Программа приёма препаратов участниками эксперимента.
Каждому добровольцу в зависимости от группы, в которую он был включён, были выданы соответствующие препараты. Препараты были упакованы в аптечные банки тёмного стекла ёмкостью 100 мл с завинчивающимися крышками. Банки были маркированы соответственно «Препарат А» (содержали таблетки аскорбиновой кислоты 0,025 г.) или «Препарат В» (содержали таблетки декстрозы моногидрата 0,5 г.).
Количество таблеток в каждой банке было просчитано, причём превышало количество таблеток, необходимых для планового курса приёма в каждой группе (для препарата «А» -100 таблеток препарата в 1 группе, 200 во второй группе, 300 в третьей группе, 200 в четвёртой группе; для препарата «В» - 100 таблеток в 4 группе). Участники эксперимента были предупреждены, что все оставшиеся после его завершения таблетки необходимо вернуть исследователю.
После завершения эксперимента из 148 участников материалы для исследования представили 129 человек (42 мужчины, 87 женщин). Из 19 человек не представивших материалы 11 были вынуждены прекратить участие в эксперименте в связи с развитием или обострением соматических заболеваний, потребовавших изменения режима и активных медицинских вмешательств (у 1 участника аппендэктомия по поводу острого аппендицита; у 1 участника холецистэктомия по поводу обострения жёлчнокаменной болезни, у 1 участника выявлен рак кишечника, у 1 участника перелом шейки бедренной кости, у 3 участников клинические проявления ИБС, нозологические причины у 4 участников не установлены), 2 не смогли участвовать в связи с командировкой, 6 прекратили участие в исследовании не мотивируя причины. Структурные изменения в группах исследования отражены в таблице 3.20.
Таблица 3.20
Количественные изменения в группах при завершении эксперимента
|
Показатель |
Участники эксперимента (n1=148; n2=129) |
|||
|
Группа 1 |
Группа 2 |
Группа 3 |
Группа 4 |
|
|
Количество участников в начале эксперимента (n1) |
37 |
37 |
37 |
37 |
|
Количество участников при завершении эксперимента (n2) |
33 |
30 |
32 |
34 |
Все таблетки, возвращенные добровольцами после окончания эксперимента, были заново пересчитаны. На основании результатов пересчёта вычисляли количество таблеток, не принятых участниками эксперимента в целом по каждой группе и внутри группы в среднем на 1 участника эксперимента.
Используя методику оценки приверженности к лекарственной терапии [14], выяснили степень приверженности участников эксперимента к приёму препаратов[6].
Результаты анализа приведены в таблице 3.21.
Оказалось, что приверженность участников эксперимента к приёму препаратов в группах существенно различалась. По шкале качества отличный результат (5 баллов) не был зарегистрирован ни в одной группе, хорошей (4 балла) оказалась приверженность лишь в группе добровольцев, принимавших в сутки однократно 1 таблетку. В группах добровольцев, принимавших 1 таблетку 2 раза в сутки и одновременно 3 таблетки 1 раз в сутки, приверженность оказалась удовлетворительной (3 балла), а в группе с приёмом 1 таблетки 3 раза в сутки - неудовлетворительной (2 балла).
Таким образом, модельный эксперимент продемонстрировал, что кратность приёма препаратов в течение суток является фактором, более существенно влияющим на приверженность пациента к приему препаратов, чем количество принимаемых одновременно препаратов. При этом назначение препаратов с кратностью приёма более 2 раз в сутки может снизить ожидаемую эффективность терапии до неудовлетворительной.
Вторым этапом эксперимента являлся анализ ответов, полученных при заполнении добровольцами авторского опросника и расчёт интегральных показателей (таблица 3.22).
Оказалось, что участники эксперимента не только приемлемо воспринимали важность лекарственной терапии, медицинского сопровождения и модификации образа жизни, но и декларировали достаточную готовность к реализации этих позиций. Женщины демонстрировали в целом более высокий, чем мужчины уровень лояльности в отношении мониторируемых позиций, причём по степени готовности к медицинскому сопровождению эти различия достигали уровня статистической значимости (Wald-Wolfowitz, р=0,029).
Таблица 3.21
Приверженность к приёму препаратов участниками эксперимента
|
Показатель |
Участники эксперимента (n =129) |
|||
|
Группа 1 |
Группа 2 |
Группа 3 |
Группа 4 |
|
|
Количество таблеток, выданных в группе, штук |
3300 |
6000 |
9600 |
10200 |
|
Количество таблеток, которое должно быть возвращено исследователю, штук |
330 |
600 |
960 |
1020 |
|
Количество таблеток, фактически возвращённых исследователю, штук |
371 |
744 |
1688 |
1323 |
|
Количество таблеток, не принятых участниками, штук |
41 |
144 |
728 |
303 |
|
Количество не принятых таблеток в пересчёте на 1 участника, штук |
1,24 |
4,80 |
22,75 |
8,91 |
|
Приверженность к приёму лекарственных средств, % |
98,7 |
97,6 |
92,4 |
97,0 |
|
Приверженность к приёму лекарственных средств по шкале качества, баллов |
4 |
3 |
2 |
3 |
Таблица 3.22
Интегральные показатели приверженности к приёму препаратов у добровольцев
|
Показатель |
Мужчины (n=42; M±SE) |
Женщины (n=87; M±SE) |
Выборка в целом (n=129; M±SE) |
|
Важность модификации образа жизни (IUWL) |
19,8 ± 1,9 |
16,3 ± 1,6* |
17,3 ± 1,9 |
|
Важность лекарственной терапии (IМТ) |
22,6 ± 1,6 |
24,2 ± 1,5 |
24,0 ± 1,6 |
|
Важность медицинского сопровождения (IMS) |
18,2 ± 2,4 |
21,2 ± 3,1 |
20,3 ± 3,2 |
|
Готовность к модификации образа жизни (АUWL) |
20,4 ± 1,9 |
22,8 ± 1,9 |
22,2 ± 1,9 |
|
Готовность к лекарственной терапии (АМТ) |
16,2 ± 2,5 |
19,6 ± 2,6 |
18,9 ± 2,6 |
|
Готовность к медицинскому сопровождению (АMS) |
16,4 ± 2,4 |
21,6 ± 2,7* |
20,4 ± 2,6 |
|
Ожидаемая эффективность модификации образа жизни (ЕUWL) |
2,23 ± 0,4 |
2,42 ± 0,4 |
2,34 ± 0,4 |
|
Ожидаемая эффективность лекарственной терапии (ЕМТ) |
2,46 ± 0,7 |
1,88 ± 0,6 |
1,98 ± 0,7 |
|
Ожидаемая эффективность медицинского сопровождения (EMS) |
3,01 ± 0,4 |
1,97 ± 0,4* |
2,18 ± 0,4 |
|
Прогнозируемая эффективность лечения (IEET) |
2,48 ± 0,6 |
2,08 ± 0,6 |
2,13 ± 0,6 |
|
Статистически значимые различия между группами (мужчины/женщины): * - по Wald-Wolfowitz р<0,05 |
|||
При сравнении результатов, полученных в модельном эксперименте, с результатами социологического исследования, между мужчинами и между женщинами раздельно (табл. 3.23) были выявлены сходные подходы добровольцев и больных к понятию важности лечебных мероприятий и готовности их выполнения, однако больные (как мужчины, так и женщины) придавали этому большее значение, чем добровольцы, при этом показатели важности модификации образа жизни у женщин и лекарственной терапии у мужчин оказались статистически различными (Wald-Wolfowitz, р=0,044 и р=0,037 соответственно).
Эти же тенденции прослеживались при сравнении приверженности к приёму препаратов в модельном эксперименте и исследовании в целом по группам (табл. 3.24).
Видно, что практически по всем позициям показатели в исследовании оказались лучшими, чем полученные в эксперименте. Как результат, прогнозируемая лучшей оказалась ожидаемая эффективность лечебных вмешательств и ожидаемая эффективность лечения в целом.
Таблица 3.23
Интегральные показатели мужчин и женщин приверженности к приёму препаратов
|
Показатель |
Мужчины, эксперимент (n=42; M±SE) |
Мужчины, исследование (n=198; M±SE) |
Женщины, эксперимент (n=87; M±SE) |
Женщины, исследование (n=297; M±SE) |
|
Важность модификации образа жизни (IUWL) |
19,8 ± 1,9 |
21,3 ± 1,4 |
16,3 ± 1,6 |
19,2 ± 1,3* |
|
Важность лекарственной терапии (IМТ) |
22,6 ± 1,6 |
27,1 ± 1,6* |
24,2 ± 1,5 |
25,3 ± 1,3 |
|
Важность медицинского сопровождения (IMS) |
18,2 ± 2,4 |
20,2 ± 1,9 |
21,2 ± 3,1 |
21,9 ± 1,9 |
|
Готовность к модификации образа жизни (АUWL) |
20,4 ± 1,9 |
19,4 ± 1,9 |
22,8 ± 1,9 |
23,2 ± 1,6 |
|
Готовность к лекарственной терапии (АМТ) |
16,2 ± 2,5 |
16,2 ± 2,4 |
19,6 ± 2,6 |
21,1 ± 2,2 |
|
Готовность к медицинскому сопровождению (АMS) |
16,4 ± 2,4 |
16,1 ± 2,2 |
21,6 ± 2,7 |
22,9 ± 2,1 |
|
Ожидаемая эффективность модификации образа жизни (ЕUWL) |
2,23 ± 0,4 |
2,18 ± 0,3 |
2,42 ± 0,4 |
2,02 ± 0,3 |
|
Ожидаемая эффективность лекарственной терапии (ЕМТ) |
2,46 ± 0,7 |
2,04 ± 0,4 |
1,88 ± 0,6 |
1,69 ± 0,4 |
|
Ожидаемая эффективность медицинского сопровождения (EMS) |
3,01 ± 0,4 |
2,76 ± 0,4 |
1,97 ± 0,4 |
1,79 ± 0,3 |
|
Прогнозируемая эффективность лечения (IEET) |
2,48 ± 0,6 |
2,21 ± 0,6 |
2,08 ± 0,6 |
1,82 ± 0,6 |
|
Статистически значимые различия между группами (мужчины/женщины): * - по Wald-Wolfowitz р<0,05 |
||||
Такие, хотя и статистически незначимые, различия представляются вполне естественными, так как в исследование были включены больные, имеющие существенный (не менее 3 лет) стаж клинически выраженной ГБ, испытывающие страдания, связанные с наличием заболевания и этим дополнительно мотивированные к лечению, в то время как в модельный эксперимент были включены лица, ещё не имеющие выраженных клинических проявлений к ГБ и фактически мотивированные к приёму препаратов личными представлениями о лечении и наставлениями исследователя.
Важным для завершающей части эксперимента было выяснить, есть ли связь между прогнозируемой индивидуальной приверженностью к лечению и продемонстрированным добровольцами качеством приёма препаратов. Для этого участники эксперимента на основании анализа результатов опросника по критерию ожидаемой эффективности лечения (IEET) были стратифицированы в три группы, с высоким, удовлетворительным и неудовлетворительным прогнозом. После чего в этих группах оценили выявленную в эксперименте приверженность приёму препаратов (табл. 3.25).
Оказалось, что количество не принятых добровольцами таблеток тем больше, чем хуже у них их прогностическое значение IEET. При корреляционном анализе по Spearman это наблюдение нашло статистическое подтверждение: была выявлена прямая сильная положительная связь между величиной показателя ожидаемой эффективности лечения IEET и числом пропущенных участниками эксперимента приёмов препаратов.
Таблица 3.24
Приверженность к приёму препаратов в эксперименте и исследовании
|
Показатель |
Выборка в целом, эксперимент (n=129; M±SE) |
Выборка в целом, исследование (n=495; M±SE) |
|
Важность модификации образа жизни (IUWL) |
17,3 ± 1,9 |
19,9 ± 1,4 |
|
Важность лекарственной терапии (IМТ) |
24,0 ± 1,6 |
25,9 ± 1,6 |
|
Важность медицинского сопровождения (IMS) |
20,3 ± 3,2 |
21,3 ± 1,9 |
|
Готовность к модификации образа жизни (АUWL) |
22,2 ± 1,9 |
22,8 ± 1,6 |
|
Готовность к лекарственной терапии (АМТ) |
18,9 ± 2,6 |
19,9 ± 2,4 |
|
Готовность к медицинскому сопровождению (АMS) |
20,4 ± 2,6 |
21,1 ± 2,4 |
|
Ожидаемая эффективность модификации образа жизни (ЕUWL) |
2,34 ± 0,4 |
2,07 ± 0,3 |
|
Ожидаемая эффективность лекарственной терапии (ЕМТ) |
1,98 ± 0,7 |
1,88 ± 0,4 |
|
Ожидаемая эффективность медицинского сопровождения (EMS) |
2,18 ± 0,4 |
1,99 ± 0,4 |
|
Прогнозируемая эффективность лечения (IEET) |
2,13 ± 0,6 |
1,99 ± 0,6 |
|
Статистически значимые различия между группами отсутствуют; по Wald-Wolfowitz во всех случаях р>0,05 |
||
Таблица 3.25
Связь показателя IEET с приверженностью добровольцами к приёму препаратов
|
Показатель |
Высокая эффективность (IEET = 1-1,99) |
удовлетворительная эффективность (IEET = 2-3,99) |
Неудовлетворительная эффективность (IEET = 4 и более) |
|
Количество добровольцев в группе, человек |
36 |
59 |
34 |
|
Количество не принятых таблеток в пересчёте на 1 участника (N штук; M±SE) |
1, 28 ± 0,84 |
2,96 ± 2,12 * 1) |
18,54± 11,52 ** 2) ; ** 3) |
|
Степень связи N - IEET; корреляция Spearman (ρs) по выборочному rs |
ρs < 0,001 rs = + 0,705 |
ρs < 0,001 rs = + 0,622 |
ρs < 0,001 rs = + 0,761 |
|
Статистически значимые различия между группами: 1) 2 группа к 1; 2) 3 группа к 1; 3) 3 группа ко 2 * - по Wald-Wolfowitz р<0,05 ** - по Wald-Wolfowitz р<0,001 |
|||
* * *
Резюмируя отметим, что экспериментальная часть исследования позволила выявить факторы, учёт и оценка которых желательны для разработки мер повышения качества антигипертензивной терапии.
К ним относятся: количество принимаемых препаратов (фактор, непосредственно влияющий на комплаентность терапии); периодичность приёма препаратов в течение суток (фактор, непосредственно влияющий на комплаентность терапии), дозы принимаемых препаратов (как фактор, способный изменять частоту развития нежелательных эффектов и опосредованно снижать комплаентность терапии), сам факт развития нежелательного эффекта (фактор, непосредственно влияющий на комплаентность терапии), наконец, общая удовлетворённость пациента самочувствием как результатом своего лечения (фактор, непосредственно влияющий на комплаентность терапии).
При реализации экспериментальной части был решен ряд прикладных вопросов, в частности - оценка и интерпретация интегральных индексов, разработанных в процессе пилотажного и эмпирического социологических исследований и апробированных в условиях модельного эксперимента.
Были разработаны следующие рекомендации:
1. Рекомендации по оценке лояльности пациента к медицинскому сопровождению (расчёт индекса EMS):
При высокой ожидаемой лояльности к медицинскому сопровождению целесообразна разработка программы наблюдения пациента, ориентированной на оптимальную, с точки зрения специалиста, частоту визитов к врачу, выполнения лабораторных и инструментальных исследований. Эффективны рекомендации по самостоятельному мониторированию пациентом артериального давления.
При удовлетворительной ожидаемой лояльности к медицинскому сопровождению целесообразна разработка программы наблюдения пациента, исходя из принципа «разумной достаточности» (минимально необходимые действия, в соответствии со стандартами лечения). Самоконтроль уровня артериального давления менее эффективен, но возможен.
При неудовлетворительной ожидаемой лояльности к медицинскому сопровождению целесообразна программа наблюдения пациента, ориентированная на посещение «по требованию». Следует учитывать, что самоконтроль уровня артериального давления маловероятен.
2. Рекомендации по оценке возможностей пациента модифицировать образ жизни (расчёт индекса EUWL):
При высокой ожидаемой эффективности модификации образа жизни оптимальны подробные рекомендации, касающиеся ограничения или отказа от вредных привычек (курение, употребление алкоголя, избыточное употребление пищи), режима диеты (структура питания, сведения о предпочтительных и требующих ограничения продуктах, включая употребление соли и жидкости) и физических нагрузок (количество и качество нагрузок, их периодичность, виды физических упражнений).
При удовлетворительной ожидаемой эффективности модификации образа жизни оптимальны конкретные рекомендации, касающиеся режима диеты (сведения о предпочтительных и требующих ограничения продуктах, о количественном употреблении соли и жидкости), физических нагрузок (вид нагрузки, продолжительность нагрузки, количество нагрузок в течение суток, недели или месяца). Следует учесть, что вероятнее всего рекомендации по ограничению или отказу от вредных привычек таким пациентом выполнены не будут.
При неудовлетворительной ожидаемой эффективности модификации образа жизни эффект от рекомендаций будет минимален. Потенциально эффективны в этом случае лаконичные конкретные рекомендации, касающиеся основных моментов режима диеты (перечислить, какие конкретно продукты необходимо исключить из рациона; указать, какое количество жидкости может быть употреблено в течение суток; рекомендовать «недосаливать» любую пищу) и физических нагрузок (например: исключить посещение сауны, совершать 30-минутные прогулки не реже 2 раз в неделю). Рекомендации по ограничению или отказу от вредных привычек выполнены не будут.
3. Рекомендации по оценке ожидаемой приверженности пациента к лекарственной терапии (расчёт индекса EМТ):
При высокой ожидаемой эффективности лекарственной терапии оптимально назначение необходимого количества препаратов в виде нефиксированной комбинации, принимаемой 1 раз в сутки. При необходимости возможно назначение препаратов с периодичностью 2 приёма в сутки. В этом случае желательно, чтобы второй приём включал не более 2 препаратов.
При удовлетворительной ожидаемой эффективности лекарственной терапии оптимально назначение препаратов 1 раз в сутки в виде комбинации, включающей фиксированные сочетания препаратов. Назначение препаратов с периодичностью 2 приёма в сутки нежелательно.
При неудовлетворительной ожидаемой эффективности оптимально проведение монотерапии, с назначением 1 препарата 1 раз в сутки, или фиксированной комбинации препаратов. Учитывая склонность таких больных к периодическому самостоятельному прекращению приёма препаратов, следует избегать назначения им лекарственных средств, требующих при отмене постепенного снижения дозы (например, высокие дозы бета-блокаторов). Назначение препаратов с периодичностью 2 приёма в сутки неэффективно.
[1] Добровольное информированное согласие участника модельного эксперимента. Я, участник исследования, зарегистрированный под № ХХХ добровольно, опираясь исключительно на собственное мнение и без принуждения, принимаю решение участвовать в программе модельного эксперимента. Мне разъяснено, что целью эксперимента является выяснение особенностей приёма таблетированных лекарственных препаратов в домашних условиях. С этой целью мне предложено принимать один или несколько таблетированных витаминных препаратов, из числа тех, что мне выдаст исследователь. Мне разъяснено, что моей основной задачей в исследовании является приём препаратов в том количестве и с той периодичностью, которую мне укажет исследователь. Мне разъяснено, что препараты будут выданы мне исследователем безвозмездно, с избытком от назначенного мне количества, но после окончания исследования я должен буду вернуть исследователю неизрасходованные мной препараты. Я подтверждаю, что согласен принимать назначенный мне препарат (препараты) в количестве, с кратностью в течение суток и с продолжительностью, указанными мне исследователем. Я осознаю, что самостоятельное, без консультации с врачом-исследователем, изменение дозировок, кратности и длительности приема назначенных мне препаратов либо частичный или полный отказ от их приема нежелательны. Мне сообщено, что при приёме любого лекарственного средства, в том числе и содержащего витамины, возможно развитие нежелательных эффектов. Мне сообщено, что для приёма каждого лекарственного средства существуют временные или постоянные противопоказания. Я подтверждаю, что исследователь ознакомил меня со всеми известными ему нежелательными эффектами и противопоказаниями, в отношении средств, приём которых мне назначен. При этом я подтверждаю, что ранее я неоднократно принимал витаминные и поливитаминные препараты без какого-либо заметного для себя вреда. Я подтверждаю, что исследователем подробно разъяснены и мне понятны все использованные в этом абзаце термины, а также мне пояснены последствия перечисленных состояний.
Я ознакомлен с тем, что перед началом эксперимента мне предложено ответить на вопросы опросника, при этом я готов с возможной для меня точностью и откровенностью письменно ответить на все вопросы, опросника, включая те, которые я считаю сомнительными или интимными. При этом исследователем мне гарантировано, что полученные от меня сведения будут использованы только в научных целях, а сами материалы будут выглядеть таким образом, что стороннему наблюдателю никаким образом будет невозможно установить мою личность. На основании изложенного, с учетом предоставленной и разъясненной мне информации, даю добровольное информированное согласие на участие в эксперименте. Дата. Подпись и её расшифровка.
[2] Соотношение участников эксперимента в зависимости от пола и возраста выбрано пропорционально распределению мужчин и женщин в основной части исследования.
[3] Самостоятельный прием участником эксперимента лекарственных средств, за исключением назначенных исследователем в период исследования.
[4] См. раздел 3.3.2 настоящей главы.
[5] Общее количество участников в группах (148) было меньшим, чем в первоначальной выборке (150).
[6] Методика оценки приверженности участников эксперимента к приёму препаратов. Приверженность участников эксперимента к приёму препаратов рассчитывали по формуле: D = [B : (A x C)] x 100, (%), где: А - число таблеток препарата (препаратов), назначенных для ежедневного приема, В - число таблеток препарата (препаратов), принятых участником исследования фактически, С - число дней лечения между визитами, D - показатель приверженности участника эксперимента к приёму препаратов. Критерии приверженности к приёму препаратов (в баллах по Шкале качества): 5 баллов (отличная) - 99-100%, 4 балла (хорошая) - 98-99%, 3 балла (удовлетворительная) - 97-98%, 2 балла (неудовлетворительная) - менее 97%.