
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
Глава 4. МЕТОД ИММУНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ НАРКОТИЧЕСКИХ ВЕЩЕСТВ И ИХ МЕТАБОЛИТОВ В РОТОВОЙ ЖИДКОСТИ «ОРАНАРК»
В последние годы на мировом рынке появилось большое количество иммунохроматографических тестов для выявления наркотических веществ в слюне. Это связано с тем, что развитые страны начали активно использовать такие тесты, замещая ими наиболее распространенные ранее ИХА-тесты по моче. Выявление наркотических веществ в слюне незаменимо в случаях, когда необходимо установить состояние наркотического опьянения. Например, в настоящее время в Европе тесты по слюне являются единственно приемлемыми для тестирования на дорогах [1]. Это связано, во-первых, с удобством их использования (неинвазивный метод, исключающий вмешательство в личную жизнь, в отличие от тестов по моче). Во-вторых, тестирование по слюне практически исключает возможность фальсификации результатов анализа или подмены образца (что очень распространено при тестировании по моче). И самое главное, в крови и слюне наркотики появляются сразу после употребления, и остаются там только в течение нескольких часов. В моче же наркотики появляются спустя несколько часов после употребления, и сохраняются до 3-х суток, когда человек уже не находится в состоянии опьянения. Результаты тестов по слюне показывают текущее состояние, когда человек находится непосредственно под воздействием наркотиков и неадекватен в поведении, что неминуемо отражается на способности управлять автомобилем (а также другими видами транспорта, сложными устройствами на производствах и т.п.).
В Европе соблюдение прав человека, в том числе права на использование рекреационных ПАВ во время отдыха, толерантность к людям, потребляющим ПАВ, являются очень важным в обществе. Поэтому здесь переход от тестирования по моче к тестированию по слюне явился основополагающим при проверке водителей на дорогах и в других ситуациях, связанных с определением непосредственного состояния опьянения.
Другие биологические образцы (моча, волосы) также считаются перспективными для различных целей: моча – для определения недавнего факта употребления ПАВ, волосы – для выявления истории наркопотребления данного человека [2].
Как уже было описано в главе 3, разработка иммунохроматографических тестов является сложной высокотехнологичной задачей. Лабораторией иммунохимии ИФАВ РАН совместно с МНПЦ наркологии разработаны экспрессные тест-системы ИХА наркотических соединений в слюне человека «Оранарк» для одновременного определения 4-х классов наркотических веществ и «Дианарк-Ора» – 6 классов наркотических веществ. Диагностические тесты характеризуются методической простотой анализа, высокой производительностью и специфичностью.
Основными иммунореагентами, полученными в ходе разработки иммунохроматографических тест-систем являлись:
1. Растворимые моноклональные антитела к исследуемому антигену, конъюгированные («сшитые») с коллоидным золотом – красителем, который можно легко идентифицировать даже в самых малых концентрациях. Такие антитела нанесены вблизи участка погружения тест-полоски в физиологическую жидкость.
2. Конъюгированные антигены исследуемых веществ с белком-носителем, жестко иммобилизованные в тестовой зоне тест-полоски.
3. Вторичные антитела к моноклональным антителам, жестко иммобилизованные в контрольной зоне тест-полоски.
В ходе разработки тест-системы на первом этапе осуществлен синтез конъюгированных антигенов производных наркотических веществ (морфина, амфетамина, кокаина и тетрагидроканнабинола) с макромолекулярными носителями (овальбумин, бычий сывороточный альбумин). Указанные наркотические вещества не содержат свободные функциональные группы для связывания с белковой матрицей. Путем ряда сложных химических реакций были поучены модифицированные производные морфина, амфетамина, кокаина и тетрагидроканнабинола, содержащие спейсер с карбоксильной группой. Синтезированы следующие соединения – 6-0-гемисукцинат морфина, d, l-1-фенил-2-карбоксиаминопропан, бензоилэкгонин, дельта-9-тетрагидроканнабинол, модифицированный реакцией азосчетания с п-аминобензойной кислотой. Перечисленные вещества использовали в качестве гаптена для конденсации с белками.
Иммунореагенты были синтезированы, протестированы, подобраны их оптимальные концентрации.
Для создания иммунохроматографической тест-полоски подобраны все необходимые материалы, их размеры и конструкция конечного иммунохроматографического теста. Слюна относится к биообъектам, которые можно собрать в ограниченном небольшом количестве; конструкция такой тест-системы должна позволять использование минимального объема образца. С этой целью используются пластиковые тест-кассеты со встронными в них тест-полосками (рис. 29).
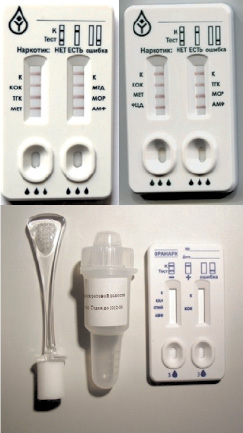
Рис. 29. Тест-системы «Дианарк-Ора» и «Оранарк»
В отличие от тестов для мочи, к тест-системам для анализа слюны предъявляются намного более высокие требования. Моча является жидкой средой, в то время как слюна – вязкой. Поэтому тесты для анализа слюны должны обладать отличными от тестов по моче характеристиками: материал составных частей тест-полоски должен давать большую скорость потока для возможности прохождения по полоске вязкой жидкости. В прокладке для образца сорбируют специальные реагенты, снижающие вязкость образца.
Также следует помнить, что кислотность слюны отличается от кислотности мочи, поэтому при производстве тест-полосок для мочи и для слюны используют различные реагенты для создания оптимальных условий иммунохимической реакции.
При использовании в качестве биообъекта слюны процедура отбора и подготовки пробы к анализу имеют принципиальное значение для успешности всего аналитического процесса. Первоначально необходимо обеспечить идентичность объекта исследования, чтобы результаты анализа отражали истинное содержание аналита в исследуемом объекте и состояние организма как источника этого объекта. В противном случае результат исследования не только теряет рациональное значение, но и может вызвать негативные последствия: врачебные ошибки, неправомерные последствия, и т.п.
Конструкция пробоотборника для слюны и материал, из которого сделана адсорбирущая часть пробоотборника, значительно влияют на конечный результат анализа. Для исключения этого нежелательного влияния необходимо выбирать материалы и конструкцию пробоотборника, руководствуюсь следующими характеристиками:
1. Способность пористого материала пробоотборника не адсорбировать определяемые вещества. В противном случае часть анализируемого вещества остается в материале пробоотборника, что отрицательно влияет на чувствительность определения.
2. Конструкция пробоотборника, позволяющая собрать и нанести на тест-кассету количество слюны, достаточное для удачного проведения теста.
Часто в качестве пробоотборника предлагается пластиковая пипетка либо стаканчик для сбора слюны. Это наиболее экономичный вариант, однако такой пробоотборник, как правило, не позволяет собрать достаточное количество слюны. Кроме того, процедура сбора слюны является неудобной для обследуемого.
Наиболее удобным для использования и позволяющим получить достаточное количество биоматериала является пробоотборник в виде губки, прикрепленной на пластиковую ручку и отдельный флакон для отжима и хранения образца (рис. 30). Адсорбирующая губка помещается в рот, отбор слюны происходит в течение 1–2 минут до полного впитывания губки. Затем губка помещается во флакон, жидкость отжимается и наносится на тест-кассету.
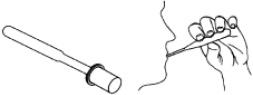
Рис. 30. Внешний вид пробоотборника и процедура сбора слюны
В результате, иммуногроматографические тест-системы «Оранарк» и «Дианарк-Ора» состоят из 3-х частей:
● пробоотборника: губка цилиндрической формы из адсорбирубщего материала с прикрепленной к ней пластиковой ручкой,
● ёмкости для сбора и хранения образца – ёмкость из бесцветного пластика, состоящая из отделения для хранения образца, перегородки для отжима жидкости ротовой полости и закручивающейся крышки,
● тестового планшета: планшет прямоугольной формы из пластика с двумя тестовыми полосками. В средней части планшета имеется две тестовых зоны прямоугольной формы с маркировками по бокам: К (контроль) и наименованием анализируемых веществ. В нижней части планшета должно находиться два отверстия овальной формы для внесения анализируемого образца (рис. 30).
Схема проведения тестирования показана на рис. 31. Она является простой и не требующей лабораторных условий и квалифицированного персонала. Отбор слюны происходит в течение 1–3 минут, а проведение самого теста занимает не более 10 минут. В итоге, вся процедура тестирования занимает 10–15 минут.
Применение иммунохроматографических экспресс-тестов для выявления наркотических веществ в слюне является единственно возможным методом обследования при освиделельствовании на состояние наркотического опьянения, например, при тестировании водителей на дорогах на постах ГИБДД (по аналогии с освидетельствованием на состояние алкогольного опьянения). Используемые иногда ИХА тесты по моче в этом случае неэффективны, т.к. показывают факт употребления наркотиков, который мог иметь место несколько суток назад.
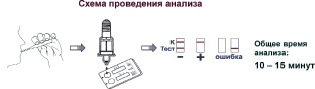
Рис. 31. Схема проведения анализа слюны
с помощью тест-систем «Оранарк» и «Дианарк-Ора»
Преимущества тест-систем «Оранарк» и «Дианарк-Ора» заключаются в следующем:
● Экспресс-тесты по слюне удобны: это неинвазивный метод, исключающий вмешательство в личную жизнь, в отличие от тестов по моче.
● Анализ слюны практически исключает возможность фальсификации результатов анализа или подмены образца, что очень распространено при использовании в качестве биопробы мочи.
● Результаты тестов по слюне показывают текущее состояние наркотического опьянения. В то же время выявление ПАВ в моче дает положительный результат в течение нескольких дней после приема наркотиков.
Иммунохроматографические тест-системы «Оранарк» и «Дианарк-Ора» позволяют выявлять метаболиты следующих групп веществ: опиаты (морфин, героин), кокаин, каннабиноиды (марихуана), амфетамин, метамфетамин, метадон, фенциклидин. Пределы обнаружения тестов и время выявления каждого класса веществ показаны в табл. 6.
Предел обнаружения тестов определяется как минимальная концентрацию аналита, при которой он может быть достоверно обнаружен. Для качественных иммунохроматографических тестов процедура определения предела обнаружениязаключается в следующем. Для каждого аналита готовили растворы определяемого вещества различных концентраций, близких к предполагаемому значению предела обнаружения. Каждый полученный стандартный раствор исследовали с помощью разработанного ИХА 30 раз. Для каждой концентрации определяли количество положительных и отрицательных результатов теста. Предел обнаружения определяли как концентрацию аналита, при которой процент положительных результатов теста равен или более 50 %. Полученные результаты определения предела обнаружения представлены в табл. 7.
Таблица 6
Чувствительность иммунохроматографических тестов
«Оранарк» и «Дианарк-Ора»
|
Группа наркотических веществ |
Предел обнаружения, |
Период выявления |
|
Опиаты |
40 |
24–36 ч |
|
Амфетамины |
50 |
24–36 ч |
|
Метамфетамины |
50 |
24–36 ч |
|
Каннабиноиды |
4 |
до 14 ч |
|
Кокаин |
20 |
до 24 ч |
|
Метадон |
30 |
24–36 ч |
|
Фенциклицин |
10 |
до 18 ч |
Не менее важной характеристикой тест-системы является ее специфичность, т.е. степень влияния на результат исследования соединений, отличных по химической структуре от анализируемого вещества, используемого как калибратор или стандарт. Чувствительность и специфичность любого иммунохимического анализа зависит от аффинности и специфичности используемых антител. Определение данных иммунохимических
характеристик очень важно для оценки получаемых результатов иммунохимических исследований и соответствия их выполнению поставленных задач.
Таблица 7
Определение предела обнаружения иммунохроматографических тестов
|
Концентрация в-ва |
n |
ОПИ |
АМФ |
ТГК |
КОК |
МЕТ |
МТД |
ФЦД |
|||||||
|
– |
+ |
– |
+ |
– |
+ |
– |
+ |
– |
+ |
– |
+ |
– |
+ |
||
|
0 |
30 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
|
–50 % ПО |
30 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
|
–25 % ПО |
30 |
25 |
5 |
23 |
7 |
25 |
5 |
30 |
0 |
27 |
3 |
25 |
5 |
29 |
1 |
|
ПО |
30 |
8 |
22 |
9 |
21 |
10 |
20 |
8 |
22 |
9 |
21 |
6 |
25 |
9 |
21 |
|
+25 % ПО |
30 |
6 |
24 |
8 |
22 |
7 |
23 |
7 |
23 |
7 |
24 |
2 |
28 |
10 |
20 |
|
+50 % ПО |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
0 |
30 |
Определение аналитической специфичности тест-систем проводили путем исследования модельных растворов, содержащих соединения, близкородственные к исследуемому веществу, и вещества, наиболее
часто встречающиеся в наркологической практике. При этом было рассмотрено влияние различных концентраций исследуемых веществ. В табл. 8 указаны концентрации веществ, при которых ИХА тест дает положительный результат. Для определяемых веществ (морфин, амфетамин и т.д.) эти цифры соответствуют пределу обнаружения теста. Для близкородственных веществ указанные значения также могут рассматриваться как предел обнаружения данного соединения.
Таблица 8
Аналитическая специфичность иммунохромато графических тестов «Оранарк» и «Дианарк-Ора»
|
Опиаты |
ПО, |
КАННАБИНОИДЫ |
ПО, |
|
|
морфин |
40 |
11-нор-Δ9 –ТГК-СООН |
4 |
|
|
этилморфин |
24 |
Каннабинол |
12500 |
|
|
6-моноацетилморфин |
40 |
11-нор-Δ8 –ТГК – СООН |
2 |
|
|
морфин 3-D-глюкуронид |
50 |
Δ8 –ТГК |
6000 |
|
|
героин |
50 |
Δ9 –ТГК |
10000 |
|
|
кодеин |
80 |
МЕТАМФЕТАМИН |
||
|
гидроморфин |
100 |
D-метамфетамин |
50 |
|
|
гидрокодон |
100 |
3,4-меилендиоксиме-тамфетамин (MДMA) |
50 |
|
|
норкодеин |
1500 |
п-гидрокси-метамфетамин |
400 |
|
|
налоксон |
– |
метоксифенамин |
> 10000 |
|
|
налтрексон |
– |
L-фенилэприн |
> 10000 |
|
|
оксикодон |
> 10000 |
D-амфетамин |
> 10000 |
|
|
AМФЕТАМИН |
МЕТАДОН |
|||
|
D-амфетамин |
50 |
метадон |
30 |
|
|
D,L-амфетамин |
125 |
доксиламин |
> 10000 |
|
|
3,4-метилендиокси-амфетамин (MДA) |
150 |
эстрон-3-сульфат |
> 10000 |
|
|
п-гидроксиамфетамин |
800 |
фенциклидин |
> 10000 |
|
|
триптамин |
1500 |
КОКАИН |
300 |
|
|
эфедрин |
400 |
Кокаин HCl |
20 |
|
|
метамфетамин |
> 10000 |
Бензоилэкгонин |
20 |
|
|
ФЕНЦИКЛИДИН |
Кокаэтилен |
25 |
||
|
фенциклидин |
30 |
Метиловый эфир экгонина |
12500 |
|
|
тетрагидразолин |
> 10000 |
Следующим этапом разработки диагностических тест-систем является их апробация в лабораторных условиях, в медицинских учреждениях и определение статистических характеристик разработанного метода. Испытание набора реагентов проводилось по методикам ГОСТ Р 15.013-94 и ГОСТ Р 51352-99 в соответствии с заявленными требованиями по разработанным инструкциям к наборам реагентов. Согласно заключению приемочной комиссии, основные характеристики Наборов «Оранарк» и «Дианарк-Ора» соответствуют проекту технических условий; опытные образцы Наборов выдержали приемочные технические испытания и могут быть представлены на медицинские испытания.
Медицинские испытания Наборов реагентов проводили согласно ГОСТ Р 15.013-94 в Московском Научно-практическом центре наркологии Департамента здравоохранения г. Москвы (МНПЦ Наркологии) и в Наркологическом диспансере № 1 г. Москвы (НД № 1). В соответствии со стандартом лабораторной практики в дальнейшем проводилась оценка достоверности результатов разработанного метода анализа. Для этого результаты, полученные при проведении анализа, сравнивались с результатами исследования референсным методом анализа – хромато-масс-спектрометрии, имеющего высокую аналитическую специфичность и надежность, что позволяет дать оценку отклонений получаемых результатов от наиболее вероятной величины.
В ходе испытаний в МНПЦ Наркологии Наборы реагентов были апробированы на 60 человеках, в том числе: на 50 пациентах, больных наркоманией, находящихся в состоянии наркотического опьянения и 10 здоровых донорах, не принимавших наркотики. Процедура анализа проходила согласно Инструкции. Затем собранные образцы жидкости ротовой полости анализировали с помощью подтверждающего метода высокоэффективной жидкостной хроматографии (ВЭЖХ) («Милихром А-02», Россия). По результатам испытаний определяли количество истинно положительных (ИП), истинно отрицательных (ИО), ложноположительных (ЛП) и ложноотрицательных (ЛО) результатов. С использованием данных значений рассчитываются статистические характеристики метода, которые характеризуют его надежность, чувствительность и специфичность.
Статистические характеристики метода рассчитываются по следующим формулам:
Чувствительность метода:
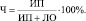
Специфичность метода:
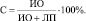
Сводные данные по количеству ИП, ИО, ЛП и ЛО результатов, а также данные по чувствительности (Ч) и специфичности (С) определения каждого класса наркотиков для тест-ситем «Оранарк» и «Дианарк-Ора», приведены в табл. 9.
Таблица 9
Статистический анализ использования наборов реагентов
«Дианарк-Ора» и «Оранарк»
|
Определяемая группа веществ |
ИП |
ИО |
ЛП |
ЛО |
Чувствительность, % |
Специфичность, % |
|
Опиаты |
33 |
65 |
0 |
2 |
95 |
100 |
|
Амфетамины |
18 |
80 |
2 |
0 |
100 |
98 |
|
Каннабиноиды |
17 |
80 |
2 |
1 |
95 |
98 |
|
Кокаин |
11 |
86 |
3 |
0 |
100 |
97 |
|
Метамфетамин |
17 |
71 |
2 |
0 |
100 |
98 |
|
Метадон |
9 |
79 |
2 |
1 |
96 |
98 |
|
Фенциклидин |
7 |
88 |
1 |
0 |
100 |
99 |
Согласно заключениям комиссий, Наборы реагентов соответствуют заявленным в Инструкции характеристикам; метод обладает высокой чувствительностью и специфичностью. Статистическая чувствительность определения наркотических веществ с помощью Наборов реагентов составляет 95–100 %, специфичность определения – 97–100 %.
Таким образом, разработанные наборы реагентов соответствуют параметрам, которые даны в инструкции по применению, медицинскому назначению, а также является удовлетворительным по эксплуатационным качествам и диагностическим характеристикам.
Набор реагентов «Дианарк-Ора» и «Оранарк», благодаря простоте и технологичности, можно использовать при:
● массовых обследованиях населения;
● освидетельствовании на состояние наркотического опьянения (водители на дорогах, «рейды» сотрудников наркополиции по ночным клубам, местам продажи и употребления наркотиков);
● определении профессиональной пригодности в ряде профессий, связанных с риском для безопасности окружающих (транспорт, опасные производства, и др.);
● в специализированных наркологических лечебных учреждениях (наркологические кабинеты поликлиники, дневные стационары, приемные отделения госпиталей и др.), при проведении медицинских осмотров, обследований и освидетельствования граждан;
● в домашних условиях для самоконтроля и контроля детей родителями.
Проведение иммунохроматографического анализа наркотиков
и их метаболитов в слюне
Проведение анализа должно осуществляться в соответствии с Инструкцией по применению наборов реагентов для иммунохроматографического анализа наркотических веществ в слюне.
1. Перед началом работы используемые Наборы реагентов должны быть выдержаны при комнатной температуре (18–25 °С) в течение 5 мин.
2. Вскрыть упаковку пробоотборника жидкости ротовой полости. Поместить губку пробоотборника (тампон) в ротовую полость, закрыть рот. Для сбора жидкости поворачивать пробоотборник внутри ротовой полости в течение 3 мин, до полного пропитывания жидкостью (рис. 30).
3. Вынуть губку пробоотборника изо рта и поместить в коллектор. Сильно нажимать на губку для максимального сбора жидкости в емкость. Извлечь губку из емкости и плотно закрутить крышку (рис. 32).
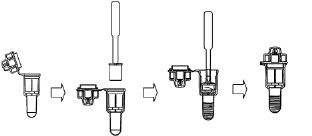
Рис. 32. Процедура отжима слюны в емкость
для сбора и хранения жидкости ротовой полости
4. Вскрыть упаковку планшета, разрывая ее вдоль прорези, извлечь планшет, поместить планшет на горизонтальную ровную чистую сухую поверхность (рис. 33).
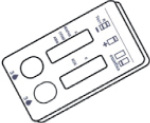
Рис. 33. Вид планшета, помещенного тестовой зоной вверх
5. Открутить крышку емкости для сбора и хранения жидкости ротовой полости и добавить в каждое отверстие планшета, предназначенное для внесения образца по три капли исследуемого материала (рис. 34).
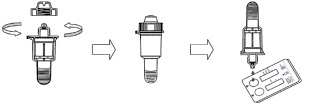
Рис. 34. Последовательность нанесения образца на планшет для проведения теста
6. Через 10 мин визуально оценить результат реакции.
7. Учет результатов.
ОТРИЦАТЕЛЬНО: Наличие по одной линии темно-розового цвета на уровне маркировок, соответствующих наркотическим веществам, а также линия темно-розового цвета на уровне маркировки К (контроль) каждой полоски. Линии могут быть яркими или бледными.
ПОЛОЖИТЕЛЬНО: Отсутствие линий темно-розового цвета на уровне маркировок, соответствующих наркотическим веществам, и наличие одной линии темно-розового цвета на уровне маркировки К (контроль) каждой полоски. Линия может быть яркой или бледной.
ОШИБКА: Отсутствие линии темно-розового цвета на уровне маркировки К через 10 мин после внесения образца. Анализ следует повторить с использованием другого планшета (рис. 35).
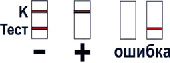
Рис. 35. Оценка результатов проведения теста
Литература
1. Driving under the Influence of Drugs, Alcohol and Medicines (DRUID), [Электронный ресурс] // – URL: http://www.druid-project.eu.
2. European Workplace Drug Testing Society (EWDTS), [Электронный ресурс] // – URL: http://www.ewdts.org/guidelines.html.
