
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
1.3. Использование современных механохимических биотехнологий с целью повышения биодоступности действующего лекарственного вещества
Широко известны биотехнологические способы переработки растительного сырья, связанные с применением сверхкритической углекислотной экстракции, сверхнизкотемпературных воздействий (–40...–50 °С) и нанофильтрации [Кершенгольц и др. 1992, 1995, 2005; Черенова и др., 1992; Ахременко и др., 1998; Тригубович, 2001]. К недостаткам известных стандартных способов переработки можно отнести тот факт, что продукция содержит растворы сахара или этилового спирта, это обусловливает высокую калорийность продуктов, нежелательные эффекты в виде повышенной раздражительности, раздражения слизистой оболочки желудка и имеют некоторые противопоказания.
На пути широкого применения метода сверхкритической СО2-экстракции стоит достаточно сложная техническая проблема – это обеспечение непрерывного внесения и выведения сырья в экстрактор и из него (непроточность реактора), также большой расход углекислоты.
На основе литературного анализа выбрана механохимическая технология переработки лишайникового сырья (рис. 11, 12), как одна из экологически чистых технологий, т.к. она не предусматривает использование органических растворителей, высоких температур и т.д.
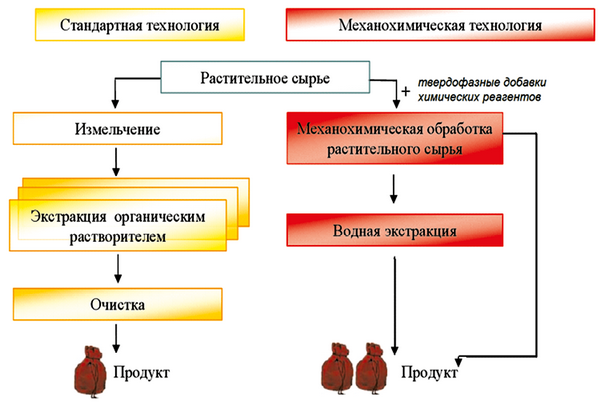
Рис. 11. Схема стандартных и механохимической технологий переработки биосырья
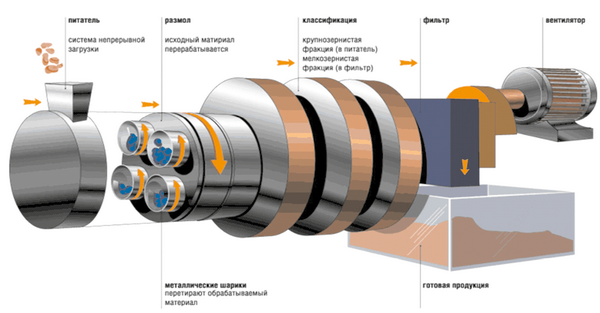
Рис. 12. Принципиальная схема механохимической установки
Остановимся на некоторых общих вопросах механохимии, в том числе классификационного характера, рассмотренных в указанном обзоре Фармацевтическое сырье в большей части имеет органическую природу. Механическая обработка ведет к многочисленным изменениям в органических веществах. Учитывая элементарные акты происходящих реакций, эти изменения можно разделить на две группы [Ломовский, 2001]. Процессы первой группы связаны с разрывом и формированием внутримолекулярных ковалентных связей, вторая группа включает процессы с разрывом и образованием более слабых межмолекулярных связей.
К первой группе механохимических реакций относятся распад молекул, оксидирование и гидролиз. В результате механической деградации молекул образуются свободные радикалы, вступающие в различные характерные химические реакции. Механохимические процессы второго типа приводят к разупорядочению, аморфизации и полиморфным переходам кристаллических решеток веществ, конформационным превращениям в составляющих решетки молекулах. Все перечисленные процессы изменяют реакционную способность и биологическую активность лекарственных веществ и могут быть использованы для создания новых эффективных технологий, получения новых активных веществ, изменения свойств лекарственных веществ и лекарственных форм [Duβinskaya, 1998;
Βoldyrev, 1994, 1996].
Прямая классификация данных по прикладной механохимии на основе рассмотрения элементарных актов соответствующих процессов не используется из-за недостатка знаний такого сорта, сложного состава реальных лекарственных форм и эмпирического характера большинства технологических публикаций. Поэтому более предпочтительна классификация данных по типам химических эффектов, используемых в механохимии.
С технологической точки зрения можно выделить следующие типы физико-химических эффектов, используемых в механохимии с прикладными целями:
– механическая активация твердых веществ,
– образование механокомпозитов с измененной реакционной способностью,
– осуществление твердофазных механохимических реакций,
– изменение биологической активности веществ и лекарственных средств,
– выделение активных компонентов при переработке растительного сырья. Рассмотрим эти эффекты.
1.3.1. Механическая активация твердых веществ
Увеличение площади поверхности механически обработанного твердого вещества часто рассматривается в качестве причины увеличения химической активности в результате обработки. Но только малая часть избыточной энергии запасается в результате образования новой поверхности, более 90 % энергии могут быть отнесены к образованию дефектов.
Измельчение твердых тел возможно до тех пор, пока размеры частиц не достигают предельных значений. После этого хрупкое разрушение становится невозможным. Более важную роль начинает играть пластическая деформация, во время которой в твердом теле происходит образование дефектов различных типов. Накопление дефектов ведет к разупорядочению кристаллической решетки и в пределе – к аморфизации вещества. Накопление энергии и образование дефектов может также приводить к образованию нестабильных полиморфных форм.
Механическая активация используется для модификации физических и химических свойств лекарственных веществ, определяющих их биологическую активность и устойчивость. Биологическая доступность и биологическая активность лекарственного средства зависит в первую очередь от растворимости лекарственного вещества. Во многих случаях биологически активные вещества имеют слишком низкую растворимость и не усваиваются организмами. С другой стороны, слишком высокая растворимость и высокая скорость растворения лекарства вредны для живого организма. Эти параметры должны быть сопоставимы с уровнем накопления соответствующих веществ в животном или человеческом организме и со скоростями метаболитических процессов.
Наиболее простой метод регулирования скорости растворения и биологической активности веществ – это формирование частиц оптимального размера. Возможно, например, эффективное улучшение биологической активности органического вещества БМК (бензимидозолил-2-метилкарбамата) формированием частиц с размерами около 220 мкм [Халиков и др., 1997]. Этот подход был применен при приготовлении антигельминтных дисперсионных препаратов.
Для измельчения частиц твердых органических веществ широко используются устройства «со свободным ударом» типа дезинтеграторов, в которых твердые частицы в газовой атмосфере обрабатываются «пальцами», прикрепленными к быстро вращающемуся диску. Аналогичным образом происходит разрушение и в струйных мельницах, когда быстро движущаяся в газовом потоке частица наталкивается на препятствие. Обычное значение площади поверхности порошкового продукта после помола органических веществ в устройствах такого типа составляет 1–10 м2/г. Предельное значение зависит от взаимной скорости частицы и поверхности рабочего органа измельчителя, числа циклов воздействия, температуры, присутствия влаги.
Низкие температуры при измельчении в замороженном состоянии обеспечивают наиболее высокие значения площади поверхности: 130 м2/г для ацетата кортизона и 400 м2/г для сапониновой кислоты [Губская, 1993]. Этим путем можно регулировать растворение некоторых лекарственных веществ, например, теофиллина [Дубинская, 1989]. Частицы теофиллина и ацетата кортизона предельных размеров около 0,1 мкм могут быть аморфизированы в последующих циклах измельчения в замороженном состоянии [Guβskaya et al., 1995].
Измельчение при низких температурах необходимо использовать, когда механическая обработка при комнатной температуре не дает результатов, как в случае коллагена и многих других материалов животного происхождения [Суходуб и др., 1993].
Аморфизация
Механическая обработка твердых кристаллических веществ в различных мельницах, и особенно в высокоинтенсивных шаровых мельницах, где реализуются условия «стесненного удара», ведет к уменьшению степени кристалличности и к аморфизации веществ.
Механическая активация клонидина [Βoldyrev, 1990] приводит к уширению рентгенографических рефлексов и уменьшению их интенсивности, что можно рассматривать как подтверждение частичной аморфизации. Такие же ситуации реализуются в случаях сульфата прастерона [Губская, 1993], сульфамидов [Савицкая, Езерский, 1991; 1992], фталазола [Чуев и др., 1991], сульфатиазола [Shakhtshneider, Βoldyrev, 1993], ацетилсалициловой кислоты [Полубояров и др., 1995]. Уширение рефлексов в дифрактограммах происходит в результате уменьшения размеров кристаллических частиц и разупорядочения структуры, связанного с нарушением системы водородных связей.
Основное практическое применение аморфизации – увеличение растворимости труднорастворимых веществ, таких как сульфамонометаксин, сульфален, сульфадимезин [Савицкая, Езерский, 1990], аспирин [Полубояров и др., 1998]. В некоторых случаях наблюдается прямая корреляция между количеством аморфной фазы и растворимостью препарата [Савицкая и др., 1991; Савицкая, 1994]. Эффект солюбилизации наиболее важен для твердых молекулярных веществ, используемых в качестве лекарств, поскольку их биодоступность в первую очередь зависит от растворимости.
Механическая модификация неорганических веществ используется в стоматологической практике. Обработка порошка кварца ведет к упрочнению включающих его композитных материалов [Ермакова, 1989], состоящих из керамической связки и абразивного наполнителя. Во время механической обработки имеют место процессы измельчения частиц связки и наполнителя и активное перемешивание. Размеры частиц связки уменьшаются до величин менее 1 мкм, керамический материал уплотняется до 150 кг/см2, затраты времени на производство сокращаются до 15 минут [Старосветский и др., 1993].
Полиморфные превращения
Известно, что некоторые органические вещества: сульфаниламиды, барбитураты, сулифатиазолы, теофиллин, ацетат кортизона [Губская, 1993; Shakhtshneider, Βoldyrev, 1993] имеют несколько полиморфных модификаций. Полиморфное превращение этих веществ связано с разрывом одних водородных и ван-дер-ваальсовых связей и образованием других. Поскольку полиморфные модификации веществ могут сильно отличаться по своим физическим и химическим свойствам, механическая обработка – возможный путь формирования новых препаратов.
Часто полиморфное превращение протекает через разупорядоченное кристаллическое состояние. Иногда новая кристаллическая фаза образуется из исходной, но становится аморфной при дальнейшем механическом воздействии.
В условиях обработки на высокоинтенсивных шаровых мельницах планетарного типа сульфатиазол [Старосветский и др., 1993, Шахтшнейдер и др., 1990; Шахтшнейдер, Хан, 1990; Shakhtshneider, Βoldyrev, 1993; Shakhtshneider, 1997] и пироксикам [Shachtshneider et al.,1997] образуют метастабильные полиморфы. Показано, что, используя различные полиморфные модификации этих веществ, можно регулировать уровень биологической активности препаратов на их основе, время действия лекарства и его стабильность.
С технической точки зрения очень важны различия между полиморфными модификациями, которые сохраняются в растворе. Эффект сохранения некоторых молекулярных ассоциатов во время растворения и дальнейшей сольватации [Леонидов, 1997] может лечь в основу новых методов изменения биологической активности лекарств.
Широко используются в технологии медицинских препаратов полимеры. Известно, что наблюдалась кристаллизация полимеров под действием механической обработки. [Вшивков и др., 1998] Макромолекулы распрямляются под действием механической нагрузки, что ведет к увеличению количества контактов между молекулами и к кристаллизации. Для кристаллического полиэтилена обнаружен
конформационный переход из гексагональной модификации в орторомбическую [Рощупкин, Барбаре, 1988; 1990].
Рассматривались последствия механической обработки наиболее используемых связок и наполнителей лекарственных форм (метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, крахмал, альгинат натрия, цеолиты, бентонит). Главным результатом было обнаружение возможности увеличения вязкости соответствующих растворов и дисперсий в 2–4 раза. Важно, что стабильность дисперсий после обработки их компонентов оставалась прежней. Таким путем можно свести количества вспомогательных материалов в составе лекарственной формы к минимуму [Егоров, Ле Кван Нгием, 1993].
Необходимо принимать во внимание возможность разрыва полимерных связей в результате механической обработки высокомолекулярного соединения. Образующиеся при распаде некоторых полимеров свободные радикалы реагируют с компонентами лекарства и изменяют их фармакологические свойства. С этой точки зрения, например, был исследован механохимический распад декстрина [Луговая, 1993].
Основные причины увеличения реакционной способности полимеров в результате механической обработки таковы:
– уменьшение размеров частиц и увеличение поверхностной энергии,
– образование свежей поверхности с нескомпенсированными связями,
– уменьшение степени упорядочения кристаллической решетки полимера,
– механическое повреждение полимерных цепей и формирование свободных радикалов,
– появление в ходе обработки микроскопических областей с повышенной температурой,
– электронная эмиссия при разрушении.
Механическая обработка лекарственных веществ и их смесей со вспомогательными веществами позволяет улучшить технологию изготовления таблетированных лекарственных форм. Активация в планетарной мельнице смесей, содержащих сухой растительный экстракт, молочный сахар, стеарат кальция, тальк и крахмал, позволяет получить таблетки с требуемой прочностью [Токпаев и др., 1997].
1.3.2. Формирование механокомпозитов и поверхностных комплексов
Механическая обработка лекарственных веществ в смеси со вспомогательными компонентами – известный метод модификации медицинских препаратов. Технологические вопросы в этом случае – какое вещество должно быть использовано для достижения определенной цели, в каком количестве оно должно быть добавлено в смесь, какой интенсивности и длительности должна быть механическая обработка. Исследования показали, что в зависимости от этих параметров реализуются различные возможности.
В особых условиях механической обработки материалов с различающимися механическими свойствами могут получаться порошки композитов, состоящих из центральной частицы, окруженной верхним слоем. Ранее на основе использования механической обработки была развита технология микрокапсулирования. Антигельминтное средство медамин с пролонгированным действием получается при нанесении полупроницаемого слоя на частицы активного вещества [Жуков и др., 1991].
В результате механической обработки смесей порошков после начального измельчения имеет место процесс агрегации микрочастиц. Формируются микрокомпозиты, состоящие из субмикронных частиц и имеющие очень развитый контакт между фазами. Частицы микрокомпозитов из некоторых веществ обладают уникальными свойствами. Например, композитные частицы из ацетилсалициловой кислоты и щелочи быстро растворяются в воде, образуя раствор лекарственного вещества [Болдырев и др., 1994; Душкин, Болдырев, 1995]. На основе этого подхода разрабатывается эффективный метод производства быстрорастворимых лекарств [Душкин и др.,1990]. Преимущества такого метода – низкие затраты на одностадийный технологический процесс, отсутствие потребления воды.
Фармакологическая активность механокомпозитов ацетилсалициловой кислоты и соды сравнивалась с активностью растворимых форм аспирина. Временные зависимости проникновения ацетилсалициловой кислоты в плазму крови кролика после орального введения механохимически произведенного медикамента и коммерческого растворимого аспирина близки друг к другу [Патент РФ 2099058, 1992].
При использовании механохимической технологии в смесь легко может быть введен третий компонент – глюкоза, фруктоза, лимонная кислота, – влияющий на скорость растворения и улучшающий потребительские свойства [Шахтшнейдер и др., 1995].
Поскольку очень мелкие частицы обычно характеризуются высокой активностью, в фармакологии традиционно используются твердые дисперсии, которые состоят из частиц активного вещества, распределенных в нейтральной растворимой матрице. Механическая обработка является альтернативным методом изготовления дисперсии, способным заменить совместное плавление лекарственного вещества и растворимого носителя.
Вещества различной природы могут служить матрицами или носителями. Например, плохорастворимое нестероидное противовоспалительное лекарство ибупрофен может быть растворено благодаря реакции как с органическими, так и с неорганическими носителями [Ягодин и др., 1991].
Разработан метод получения твердых растворов некоторых лекарственных веществ в высокоэффективных механических активаторах [Βoldyrev et al., 1993]. Например, механическая обработка сульфатиазола с поливинилпирролидоном переводит кристаллическое вещество в аморфное состояние. Процесс сопровождается образованием водородных связей между молекулами сульфатиазола и полимерной матрицей. Растворимость препарата меняется вместе с весовым содержанием полимера. Массовое соотношение полимера к лекарственному веществу, равное 1:3, дает наиболее высокую растворимость [Бабиевская и др., 1993; Βoldyrev et al., 1994].
Когда лекарственный компонент механически обработанной смеси измельчается до молекулярного уровня, могут получаться так называемые привитые или поверхностные комплексы. Образуются водородные связи между карбонильными и аминогруппами лекарственного вещества и гидроксильными группами полимерного носителя. Привитые комплексы характеризуются более высокими величинами растворимости и скорости растворения. Пример таких систем – салициловая кислота, клонидин, нозепам – целлюлоза [Ягодин, Болдырев, 1989; Ягодин и др., 1991]. Хитин и хитозан также могут использоваться как носители в приготовлении твердых растворов лекарств [Дубинская и др., 1988].
Молекулярные агрегаты, соединенные водородными связями в твердом состоянии, могут сохраняться и в растворе после растворения, иногда на долгое время
[Леонидов, 1997].
Предельная степень растворения вещества является параметром термодинамическим и не должна зависеть от степени дефектности его кристаллической решетки, по крайней мере после достижения равновесия при растворении. Поскольку в данном случае растворяется уже не само вещество, а его комплексы, появляется возможность увеличения растворимости лекарств. Исследовались превращения лекарственных веществ при совместной механической обработке с наполнителями. В результате обработки сульфатиозола, смешанного с поливинилпирролидоном, рефлексы порошковой рентгенограммы исчезают полностью. По-видимому, вещество распределяется по носителю [Βoldyrev, 1994] и вступает с ним в химическое взаимодействие. Исследованы такие системы, как ибупрофен – полиэтиленгликоль [Shakhshneider et al., 1994], ибупрофен и парацетамол с органическими и неорганическими носителями [Vasilchenko et al., 1997].
По скорости растворения эквимолярная смесь ибупрофен – полиэтиленгликоль показывает наилучший результат по сравнению с образцами, полученными выдерживанием совместного расплава длительное время. Механическая обработка смеси парацетамол – микрокристаллическая целлюлоза обеспечивает существенное увеличение начальной скорости растворения.
Образование молекулярных комплексов лекарственных веществ с полимерами может приводить как к уменьшению, так и увеличению растворимости [Дубинская, 1990], например, бензимидозола с микрокристаллической целлюлозой [Халиков и др., 1995] и другими полимерами [Kutlymuratov et al., 1997]. Механическая обработка низкомолекулярного алкалоида – гидробромида лаппаконитина – с целлюлозой дает пролонгированную форму лекарства [Khalikov et al., 1995].
Было показано, что при совместной механической обработке может обеспечиваться стабильность состава лекарства. Механическая обработка чистого алкалоида ведет к реакции перегруппировки с формированием амида антраниловой кислоты [Халиков, Арипов, 1995]. Механическая обработка смесей с пектиновой кислотой сохраняет свойства алкалоида [Khalikov, Aripov, 1995].
Разработан новый ветеринарный препарат в форме водного раствора комплекса йода с поливинилхлоридом и поливиниловым спиртом [Чуев, 1991].
Бензимидозол-2-метилкарбомат (БМК) и его производные являются перспективными антигельминтиками, но имеют слишком низкую растворимость. Совместная механическая обработка БМК с натуральными и синтетическими полимерами (пектин и полиметакриловая кислота) [Халиков и др., 1995; Khalikov et al., 1995] ведет к частичной аморфизации БМК. Имеет место реакция аминогрупп БМК и С = О и ОН-групп полимеров [Khalikov et al., 1996]. Молекулярная масса полиметилметакриловой кислоты уменьшается с 8000 до 820 [Кутлымуратов, 1997]. Степень растворения этого препарата в условиях среды желудка – 90 % [Халиков, 1995]. Технология производства антигельминтных препаратов нового поколения разработана на основе полученных результатов [Кутлымуратов, 1997].
Изменение растворимости антигельминтных препаратов типа бензимидозола может быть обеспечено реакцией с проантоцианидинами растительного происхождения [Халиков и др., 1995].
Другое приложение механохимических реакций с полимерами – это иммобилизация лекарств. У некоторых антигельминтных, антихолинэстеразных, антиаритмических лекарств избыточная растворимость может быть понижена после механохимической реакции с полимерами синтетической и растительной природы [Халиков, Арипов, 1993], например, с пектином [Халиков С.С. и др., 1992].
Внедрение некоторых веществ в слоистые неорганические матрицы используется в технологии материалов с регулируемой скоростью выделения компонентов в воду. Маханохимически приготовленный интеркалят гидроксида лития в оксиде алюминия [Исупов и др., 1990] может использоваться для получения психотропных литиевых препаратов с длительным действием [Исупов, 1998].
1.3.3. Механохимический синтез
Вопрос о том, каким образом обеспечивается повышение подвижности компонентов твердой смеси, достаточное для образования новых соединений в условиях механической обработки смесей твердых веществ, остается непонятным. Рассматривается возможность осуществление двух основных механизмов:
– перемешивание реагентов на молекулярном уровне под механическим воздействием,
– образование микрокомпозитов, исключающее необходимость транспорта компонентов на дальние расстояния и поверхностное взаимодействие микроскопических частиц.
В свое время было показано, что механохимический синтез может успешно использоваться в фармацевтической промышленности. Он может помочь в создании новых технологических процессов, экономически более эффективных и экологически чистых.
Данные относительно синтеза лекарственных веществ классифицируются далее на основе отнесения к типам наиболее изученных реакций.
Реакции нейтрализации
Один из наиболее используемых методов увеличения растворимости биоактивных органических кислот – это превращение в солевую форму реакцией нейтрализации щелочным веществом. Разработано твердофазное механохимическое производство щелочных и щелочноземельных солей аскорбиновой кислоты и кальциевых солей аланиновой и фолиевой кислот [Чуев и др., 1990; 1991]. Исследованы механохимические реакции нейтрализации различных органических кислот (бензойной, салициловой, лимонной, себациновой, индолацетиловой и аскорбиновой) гидроксидами и карбонатами натрия и калия, углекислым кальцием [Dushkin et al., 1991; 1994]. Эквимолярное введение щелочи приводит к полному превращению кислоты в соль. Рентгенофазовый анализ подтверждает образование кристаллических солей.
Проведено сравнение твердофазных механохимических и обычных жидкофазных технологий [Βoldyrev, 1996]. Бензойнокислый натрий обычно получается в медицинской промышленности нейтрализацией кислоты углекислым натрием в водном растворе. Технологический процесс включает следующие стадии:
1) растворение кислоты в воде;
2) нейтрализация углекислым натрием;
3) фильтрация;
4) сушка;
5) измельчение;
6) упаковка.
В блок-схеме механохимической технологии имеются только следующие операции:
1) смешивание твердых компонентов;
2) механическая обработка;
3) упаковка.
Технологическая скорость механохимического процесса по сравнению с твердофазным значительно выше.
Чтобы получить 1 кг бензоата натрия, требуется 6 кг воды. В механохимической технологии вода не используется, нет и проблем со стоками.
Для производства 10 кг соли в час требуются: два химических реактора объемом 3 м2, оборудование для фильтрации, вакуумная сушилка и мельница. Необходимое оборудование для механохимического процесса с производительностью 100 кг в час – механохимический реактор, например, мельница-активатор виброцентробежного типа ВЦМ, и питатель.
Синтез амидов (реакции ацилирования)
Смеси порошков ароматических аминов и карбоксильных кислот реагируют в твердом состоянии механохимически с формированием амидов. В условиях деформационного сдвига выход достигает 50 %. Скорости превращения – в 100 000 раз больше, чем в жидкофазном процессе [Леонтьев и др., 1992]. Для орто-фенилендиамина, наряду с синтезом амида, происходит циклизация с формированием соответствующего бензимидазола. Аналогичная реакция имеет место в условиях ударной механической обработки в интенсивной шаровой мельнице. Растворители при получении не используются, аморфный продукт реакции при необходимости может быть перекристаллизован и очищен [Халиков, 1993]. Выход уменьшается в ряду: бензойная, монохлоруксусная, малеиновая кислота с уменьшением pK [Халиков и др., 1993].
Механохимическая реакция фталевого ангидрида и сульфатиазола в планетарной шаровой мельнице приводит к образованию фталилсульфатиазола. Выход близок к теоретическому. Обычные для жидкофазного синтеза побочные продукты в полученном веществе не содержатся [Чуев и др.,1989; Chuev et al., 1991].
Подобие кристаллических структур реагирующих веществ способствует реакции. Ромбические кристаллы малеинового ангидрида и диаминдифенилсульфона, моноклинные кристаллы фталевого ангидрида и парафенилендиамина взаимодействуют почти количественно. Кристаллы малеинового ангидрида и парафенилендиамина, имеющие различные структуры, реагируют с низкой скоростью [Волков и др., 1990].
Исследованы реакции хлоргидрата бензимидазол-2-метилкарбамата с полиметакриловой кислотой [Кутлымуратов и др., 1997] и малеинового ангидрида с мочевиной [Чуев и др., 1992]. В последнем случае была обнаружена удивительно высокая селективность синтеза цис-изомера.
Примеры успешного применения механохимии демонстрировались при разработке растворимых форм витаминов E, А и K, при синтезе фосфорных эфиров тиамина. Очень высокая селективность выхода продукта наблюдалась в реакции замещенных гидразинов с глутаровым альдегидом при формировании гидразидов [Бузов и др., 1993].
Другие органические и неорганические реакции
Рассматривались механохимические реакции полимеров, используемых в медицинских технологиях в качестве носителей и вспомогательных веществ, например, разложение декстрина [Луговая и др., 1993]. Пектин также разлагается при интенсивной механической обработке и теряет свойства электролита [Халиков и др., 1995].
В результате твердофазного механохимического процесса под действием сдвиговой механической деформации возможно формирование хитозанового и карбоксиметилового эфиров хитина и хитозана [Зеленецкий и др., 1993], также как
и карбоксиметилирование целлюлозы в шаровых мельницах и аттриторах [Galotshkin et al., 1998; Базарнова, 1999; Ломовский, Фадеев, 2000].
При воздействии сдвиговой деформации на смеси твердых аминокислот происходит синтез полипептидов. В отличие от реакции в растворах и расплавах в механохимическом процессе преимущественно формируются линейные продукты, а не циклические соединения типа диацетопиперазина [Яковлева, 1990].
Молекулярные комплексы глицирризиновой кислоты (компонента солодки) с нестероидными жаропонижающими лекарственными веществами – ацетилсалициловой кислотой и вольтареном (ортофеном) – в мольных отношениях 1:1 и 2:1 образуются в результате двухминутной механической обработки в шаровой мельнице [Dushkin et al., 1999]. Комплексы этого типа обеспечивают перенос активных компонентов в живых организмах.
При обработке в планетарной мельнице галогенидов ароматических соединений, содержащих разные галогены, имеют место реакции обмена галогенами [Душкин и др., 1990].
Сообщалось о возможности окисления сложного имидазолина персульфатом калия и диоксидом свинца [Dushkin et al., 1993].
1.3.4. Изменение биологической активности
Отмечалось, что изменение реакционной способности механически обработанных твердых веществ часто нельзя объяснить только изменением размера частиц. Например, площадь поверхности порошка сульфамонометоксина [Савицкая и др., 1990] увеличивается при обработке в 6 раз, тогда как скорость растворения лекарства увеличивается в 8,6 раз. Удивительно, что с коэффициентом 1,4 увеличивается и растворимость, с термодинамической точки зрения равновесная растворимость должна оставаться постоянной.
Число мышей, выздоровевших через 10 дней после введения механически активированного сульфамонометоксина, вдвое выше, чем в контрольной группе.
Механическая активация противогрибкового лекарственного средства гризеофульвина с некоторыми носителями (картофельный крахмал, полиэтиленгликоль, хитозан) увеличивает растворимость и биодоступность вещества. Концентрация гризеофульвина в крови кроликов, получавших механически активированный препарат, повышается в 1,5 раза [Бабакина и др., 1991].
Свойства алкалоидов растительного происхождения изменяются после механической обработки [Халиков, Арипов, 1995].
Механическая активация может изменять каталитическую активность белковых ферментов. Необратимая механическая инактивация наблюдалась после обработки порошков некоторых протеаз, таких как трипсин и субтилизин [Чижиков, Балабудкин, 1995]. Некоторые данные указывают на конформационные изменения в молекуле белка как причину эффекта.
Биологическое действие тималина (комплекс полипептидов с иммуно-модулирующим действием) увеличивается при механической обработке [Орел и др., 1994]. Коэффициент увеличения зависит от дозы поглощенной механической энергии и изменяется в 8 раз [Орел и др., 1993]. Причины эффекта неясны, возможно, что необратимые изменения в структуре тималина способствуют увеличению иммунного ответа. В любом случае эффект имеет большую практическую ценность [Orel et al., 1993].
Антиканцерогенный эффект антрациклинового антибиотика доксорубицина может быть усилен механической активацией [Орел и др., 1998]. Обработка ведет к разупорядочению вторичной структуры антибиотика, связанной со взаимным расположением молекул, и к активации процессов с участием свободных радикалов, разрушающих раковые клетки [Орел и др., 1998].
О причинах изменения биологической активности механически активированных лекарств известно очень мало. Поэтому в этой области особенно важны экспериментальные данные.
1.3.5. Выделение активных компонентов
при переработке растительного сырья
Экстракция – обязательная стадия производства лекарств из растительного сырья. Практика показывает, что существует оптимальный размер частиц порошка растительного сырья, который обеспечивает полноту извлечения и чистоту продукта.
Основная часть биологически активных веществ растения находится в клетках. Для максимально эффективной экстракции клетки должны быть разрушены. Использование механической обработки эффективно для экстракции из кожуры апельсина таких нерастворимых флавоноидов, как гесперидин и диосмин [Бандюкова и др., 1995].
Скорость экстракции и выход продукта определяются диффузией растворителя в частицах растительного сырья. Механическая обработка может использоваться для ускорения диффузионных процессов. Обработка сырья непосредственно в растворителе позволяет упростить экстракционный процесс, уменьшить затрачиваемое на экстракцию время в несколько десятков раз. Примером может служить экстракция кумаринов этиловым спиртом [Балабудкин, Агаев, 1993].
Некоторые биологически активные вещества невозможно или неприемлемо дорого синтезировать. Высокая цена алкалоидов и гликозидов растительного происхождения – результат их низкого содержания в сырье и сложности промышленной технологии извлечения. Общепринятая технология производства лекарственных веществ из растительного сырья – многоступенчатая экстракция. Сырье обрабатывается рядом органических растворителей различной полярности. Разбавленные растворы извлеченного вещества концентрируются в твердый экстракт, используемый как активная составляющая лекарства.
Технология твердофазной механохимической экстракции состоит из механической обработки порошковых смесей растительного сырья и твердых адсорбентов различной химической природы. Биологически активное вещество в условиях механической обработки перемещается по частице сырья, сорбируется на адсорбенте и может быть легко выделено, сконцентрировано и высушено [Lomovsky et al., 1999].
Эффективность технологии демонстрируется на выделении дитерпеновых акалоидов из Aconitum и сесквитерпеновых лактонов из Inula helenium. Селективность механохимической экстракции, превышающая селективность выделения путем жидкостной экстракции, показана на выделении сердечных гликозидов из желтушника Сheranthoides [Ломовский и др., 2000].
Показано, что в результате механической обработки смеси алкалоида и твердого адсорбента с кислотными центрами на поверхности происходит образование солевых форм алкалоида [Ломовский, 1999].
Растительное сырье – сложный комплекс химических веществ, содержащий соединения как растворимые, так и нерастворимые в воде. Данное обстоятельство сильно осложняет технологию химической переработки, особенно в случае многотоннажных сырьевых источников, таких как кора или зелень древесины. В основе, например, существующих технологий переработки коры хвойных пород лежит принцип последовательной экстракции полезных веществ органическими экстрагентами возрастающей полярности. Обычно экстракция осуществляется в три ступени, что позволяет, например, последовательно выделить:
1) гексаном при 25–30 °С – липиды (смолистые вещества);
2) этилацетатом – фенокислоты, флавоноиды, краситель;
3) водой при высоких температурах – танниды (дубильные вещества).
Прямая водная экстракция коры, содержащей нерастворимые липидные смолистые компоненты, неэффективна.
Механохимическая экстракция коры позволяет в одностадийном процессе выделить водорастворимые вещества в предельных количествах, не проводя предварительное отделение липидов органическими растворителями, снизив температуру и длительность экстракции [Ломовский, Белых, 2000].
Что касается лекарственных препаратов древесного происхождения, необходимо обратить внимание, что механическая обработка расширяет степень утилизации целлюлозосодержащего сырья [Бабкин, 1994; Ломовский, 1994]. Механохимическое разрушение целлюлозы в присутствии небольших количеств кислоты может рассматриваться как перспективный метод получения микрокристаллической целлюлозы и полисахаридов [Иванова и др., 1991]. Метод имеет преимущества: уменьшение длительности процесса с нескольких часов до минут, уменьшение потерь, исключение системы регенерации кислоты и очистки гидролизатов [Бабкин и др., 1997].
Комплексы веществ, извлеченных из растений, могут быть механохимически преобразованы в биологически активные лекарственные [Прибыткова, 1999]. Эмодин и другие гидроксиантрахиноны из Rumex tianschanicus взаимодействуют с аминокислотами и гидроксиламинами с формированием препаратов, обладающих противораковым действием [Прибыткова, Душкин, 1995; Прибыткова и др., 1996]. Обработка биологически активного комплекса веществ из Salsola collina обеспечивает повышение эффективности его гепатопротекторного действия [Прибыткова и др., 1998].
Для объяснения наблюдаемых эффектов могут привлекаться различные представления. Высокие скорости перемещения молекул биологически активных веществ в ходе механической обработки твердофазных смесей объясняются их механически активированной, баллистической диффузией. Альтернативные представления исходят из обязательного присутствия воды в клетках растительного сырья. В условиях механической обработки такая вода может переходить в сверхкритическое состояние, обеспечивающее ускоренный транспорт растворенных веществ [Ломовский и др., 1998; Кальченко и др., 1999].
Механическая обработка растительного, в частности, зернового, сырья совместно с биологически активными веществами может использоваться для изменения скорости растворения веществ. В зависимости от состава растительного сырья и типа механической обработки – ударного или сдвигового – скорость выделения карбамида из его смесей с сырьем может изменяться в сотни раз.
В работе Е.С. Метелевой [Метелева, 2010] указывается, что для увеличения растворимости и скорости растворения лекарственных средств часто используют способы, основанные на образовании аддуктов/комплексов лекарственных веществ с водорастворимыми синтетическими или природными полимерами или олигомерами. Эти материалы получают с использованием жидко-фазных технологий –
из растворов или расплавов, что имеет существенные ограничения, связанные с термической стабильностью и совместной растворимостью веществ.
В ИХТТМ СО РАН, благодаря развитию методов химии твердого тела, успешно разрабатывается механохимический подход для твердофазного синтеза органических соединений и получения быстрорастворимых композиций для фармации, обладающий преимуществами по сравнению с традиционными жидкофазными процессами. В этом направлении весьма перспективным названо исследование механохимически полученных композиций лекарственных веществ (ЛВ) с природными полисахаридами и родственными соединениями. Автор сообщает, что при механохимическом получении таких композиций возможен довольно широкий спектр физико-химических взаимодействий веществ – образование химических ковалентных и ионных связей, межмолекулярных/супрамолекулярных комплексов, фазовые трансформации, изменение степени кристалличности и пр. Это позволяет в широких пределах варьировать свойства получаемых материалов для достижения желательных характеристик.
Среди разнообразия природных полисахаридов и растительных гликозидов наибольший интерес представляют уже использующиеся в медицинской и пищевой промышленности хитозан, арабиногалактан (из лиственницы Сибирской и Гмелина), фибрегам (из камеди акации), декстраны (10, 30 и 70 кДа), гидроксиэтилкрахмал (200/0,5), а также глицирризиновая кислота.
Были исследованы твердофазные реакции хитозана с ароматическими карбоновыми кислотами, полученные продукты охарактеризованы по степени замещения/присоединения, характеру взаимодействий; механохимический способ получения композиции арабиногалактана, фибрегама, декстранов, гидроксиэтилкрахмала, а также глицирризиновой кислоты и малорастворимых лекарственных веществ и обнаружено значительное (до 102 раз) повышение водорастворимости лекарственных веществ из полученных композиций; проанализирован характер взаимодействий макромолекул арабиногалактана и глицирризиновой кислоты с рядом малорастворимых лекарственных веществ в составе твердых композиций и в их растворах; изучены механохимические превращения макромолекул полисахаридов, происходящие при различных условиях механической обработки, обоснованы предпочтительные условия получения твердых композиций; проведено сравнение различных полисахаридов, глицирризиновой кислоты и бета-циклодекстрина в качестве комплексообразователей с молекулами малорастворимых лекарственных веществ.
На основании проведенных в НИОХ СО РАН токсико-фармакологических испытаний ряда полученных в настоящей работе композиций показана возможность многократного (до 101–102 раз) снижения действующих доз лекарственных веществ при сохранении их базовой активности.
Обоснована перспективность использования механохимического пути получения композиций малорастворимых лекарственных веществ с полисахаридами и глицирризиновой кислотой для создания лекарственных средств повышенной эффективности и уменьшения степени выраженности нежелательных побочных эффектов [Душкин и др., 2008].
Этим же автором [Душкин и др., 2008] в составе коллектива ученых из институтов Сибирского отделения РАН (Институт химии твердого тела и механохимии, Новосибирский институт органической химии, Институт химической кинетики и горения, Иркутский институт химии им. А.Е. Фаворского) ранее была исследована возможность механохимического получения водорастворимых комплексов растительного полисахарида арабиногалактана и малорастворимых лекарственных веществ (сибазона, мезапама, индометацина и азалептина), их молекулярная динамика методом ЯМР-релаксации в растворах, а также некоторые фармакологические свойства в сравнении с исходными лекарственными веществами.
В работе [Бычков и др., 2010] другого коллектива ученых из Новосибирска (Институт химии твёрдого тела и механохимии СО РАН, НОЦ «Молекулярный дизайн и экологически безопасные технологии», Институт химической биологии и фундаментальной медицины СО РАН) методом просвечивающей электронной микроскопии и химическим анализом изучено влияние механической обработки (стесненного удара) на морфологию клеточной стенки дрожжей Saccharomyces сerevisiae и масличной пальмы Elaeis guineensis. Представлены особенности разрушения клеточной стенки. Отмечено, что изменение надмолекулярной структуры биополимеров клеточной стенки наблюдается у менее устойчивой клеточной стенки дрожжей.
Из выводов, сделанных в статье, следует, что в ходе работы выявлены и проанализированы процессы, происходящие при механической активации в клеточных стенках дрожжей и гроздей масличной пальмы Elaeis guineensis.
Установлено, что тип процессов зависит от выбранного сырья и структурных особенностей клеточной стенки. Увеличение реакционной способности, происходящее в результате механической активации, определяется механическим разрушением клеточной стенки, разупорядочением надмолекулярных структур биополимеров клеточной стенки. В результате механической активации дрожжевой биомассы происходит разупорядочение надмолекулярной структуры клеточной стенки, увеличивается дефектность глюканового слоя, вследствие чего значительно возрастает реакционная способность структурообразующего компонента – глюкана. В результате механической активации волокон гроздей масличной пальмы Elaeis guineensis разрушение материала идет по границе клеточных стенок. В случае низкой интенсивности механического воздействия разрушение происходит путем образования осколков вдоль волокон стенки, а в случае высокой интенсивности механической активации – путем расслоения клеточных стенок. Ученые считают, что, по-видимому, при механической активации ультраструктура слоёв клеточной стенки Elaeis guineensis не изменяется, однако слои могут смещаться друг относительно друга.
Румынские ученые из Бухареста (Analytical Chemistry Department, Faculty of Pharmacy, UMF Carol Davila, Traian Vuia Streetno. 6, Βucharest, Romania) изучали вопросы растворения комплексов включения репаглинида (орального антидиабетического препарата, практически нерастворимого в воде) с β-циклодекстрином и его производными [Nicolescu et al., 2010]. Целью работы было улучшение растворимости фармакона в воде, основанное на образовании комплексов включения с β-циклодекстрином (β-CD), гидроксипропил β-циклодекстрином (HP-β-CD) и частично (выборочно) метилированным β-циклодекстрином (RAMEΒ), а также изучение соответствующих характеристик. Учитывая липофильность цвиттерионной структуры репаглинида, все определения проводились в фосфатных буферах (pH = 6). Исследования показали увеличение растворимости репаглинида в присутствии β-CD, также как и его производных, HP-β-CD и RAMEΒ, в зависимости от типа циклодекстрина. В заключение сообщается, что на основании полученных данных комплексы репаглинида с β-циклодекстрином, гидроксипропил β-циклодекстрином и частично метилированным β-циклодекстрином можно расположить по убыванию стабильности следующим образом: HP-β-CD > RAMEΒ > β-CD.
Коллектив новосибирских ученых из Института химии твёрдого тела и механохимии СО РАН и из НОЦ «Молекулярный дизайн и экологически безопасные технологии» при НГУ занимался вопросами механохимического синтеза наноструктурированных фаз мелоксикама [Мызь и др.]. Наноструктурированные фазы мелоксикама представляют собой структурно однородный кристаллический материал, который содержит два нейтральных строительных блока, находящихся в определенных стехиометрических соотношениях и удерживающихся вместе одним или комбинацией нескольких типов межмолекулярных взаимодействий. В работе получены наноструктурированные фазы мелоксикама с 17-ю карбоновыми кислотами механохимическим методом. Механическую обработку компонентов проводили растиранием вручную в агатовой ступке или в вибрационной мельнице при комнатной температуре в течение 20–30 минут, как в сухом виде, так и с добавлением небольших количеств растворителя. Полученные образцы исследовали методами рентгенофазового анализа и ИК-спектроскопии. Для нескольких соединений методами монокристальной рентгеновской дифракции удалось расшифровать структуру получившихся смешанныхкристаллов. В качестве примера в работе приведена структура наноструктурированной фазы мелоксикама с адипиновой кислотой (соотношение 2:1). Показано, что каждая молекула адипиновой кислоты в кристалле лежит на центре инверсии и связывается через водородные связи N–H·O и O–H·N с двумя молекулами мелоксикама. В результате слой молекул адипиновой кислоты располагается между двумя слоями молекул мелоксикама, образуя двойные слои.
Эксперименты доказали, что при добавлении разных растворителей можно получать различные наноструктурированные фазы для одних и тех же компонентов. Были измерены скорости растворения для нескольких смешанных кристаллов и показано, что скорость растворения смешанных кристаллов превышает таковую для исходного мелоксикама. Ученые отмечают, что полученные результаты можно использовать при разработке новых лекарственных форм на основе наструктурированных фаз мелоксикама с улучшенными свойствами. Очевидно, что одним из приоритетных направлений фундаментальных и прикладных исследований в современной онкологии является создание новых противоопухолевых препаратов. Отсутствие избирательности действия известных препаратов и их высокая общая токсичность вызывает как дальнейший поиск новых соединений, так и усовершенствование лечебных форм существующих лекарств.
Известно, что в результате совместной механической активации пироксикама с ПВП были получены нанокомпозиты с повышенной скоростью растворения и растворимостью лекарственного вещества [Шахтшнейдер и др.]. Композиты пироксикам-МКЦ также проявили повышенную скорость растворения лекарственного вещества. При этом концентрация пироксикама в растворе превышала незначительно концентрацию лекарственного вещества в случае механически активированного чистого пироксикама, но образцы с МКЦ, в отличие от чистого лекарственного вещества, оказались более стабильны и сохраняли пироксикам в активной форме в течение длительного времени. Получены также композиты пироксикам-ПЭГ. Установлено, что в результате взаимодействия компонентов механическое диспергирование в присутствии ПЭГ приводит к повышению скорости растворения и растворимости пироксикама по сравнению с физическими смесями компонентов.
Относительно композитов пироксикам-SiO2 указывается, что их растворимостьпревышала растворимость исходного пироксикама. При этом наибольшую скорость растворения и растворимость (почти в 3 раза превышающую растворимость исходного лекарственного вещества) проявили образцы с соотношением компонентов 1:1, полученные в мельнице SPEX 8000. Для образцов, обработанных в АГО-2, характерно более медленное растворение, тем не менее, достигнутые значения растворимости в 2 раза превышали растворимость исходного пироксикама.
Полученные механокомпозиты пироксикама с MgO также показали повышенную растворимость по сравнению с исходным лекарственным веществом. Для смесей, обработанных в мельнице SPEX 8000, были получены кривые с максимумом, для которых характерна высокая скорость растворения в начальный момент времени. На кривых растворения рентгеноаморфных образцов с соотношением компонентов 1:3, полученных обработкой в мельницах SPEX 8000 и АГО-2 в течение 30 минут, максимумов не наблюдалось. Образцы проявили максимальную растворимость, большую, чем исходный пироксикам, в 8 и 6 раз, соответственно.
О нанокомпозитах индометацина сообщается следующее. Индометацин-Al2O3: растворимость почти всех полученных образцов была на уровне 0,015–0,02 мг/мл, т.е. в 3 раза больше растворимости исходного лекарственного вещества. Композит индометацин-SiO2 показал значительное увеличение растворимости действующего начала по сравнению с исходным лекарственным веществом. Наибольшая скорость растворения и растворимость наблюдались для образцов с соотношением компонентов индометацин – SiO21:3. Так, кажущаяся растворимость образца индометацин – SiO21:3, полученного обработкой в мельнице SPEX 8000 в течение 30 минут, достигала 0,14 мг/мл, т.е. в 28 раз превосходила растворимость исходного лекарственного вещества.
В заключение отметим, что применение механохимических подходов в фармацевтике и медицинской промышленности имеет перспективы, поскольку это позволяет проводить некоторые технологические процессы доступными и экологически чистыми методами без использования дополнительных химических реагентов и растворителей.
Анализ литературы также свидетельствует о том, что современная отечественная и зарубежная сырьевая база предоставляют широкие возможности для получения огромного разнообразия механохимических комплексов различных фармаконов как на основе широко известных эксипиентов, традиционно применяемых в качестве вспомогательных веществ при изготовлении твердых лекарственных форм, так и на базе новых, не задействованных ранее источников. В роли комплексообразователей могут выступать природные высокомолекулярные соединения из растительного сырья различного состава (полисахариды на основе целлюлозы и ее производных, гемицеллюлозы, крахмалы, пектиновые вещества, лигнины, танины, белки и др.), а также другие органические и неорганические вещества.
На основе литературного обзора, нами выбрана механохимическая активация слоевищ лишайников с фармаконом, которая предполагает создание низкодозовых биопрепаратов бинарного назначения: повышенных сорбционной активности и биологической доступности и, как следствие, высокой адаптогенной активности биокомплексов для профилактики и лечения заболеваний человека, вызванных экологическими (природными и/или техногенными) и социальными стресс-факторами.
