
Научная электронная библиотека
Монографии, изданные в издательстве Российской Академии Естествознания
3.2. Биохимический состав механоактивированного биокомплекса лишайника с родиолой розовой
Был проведен хроматомасс-спектрометрический анализ фракции низкомолекулярных органических веществ механохимически активированных корней и корневищ Rhodiola rosea и смеси слоевищ лишайника рода Cladonia и Rhodiola rosea, в массовом соотношении 10:1, предварительно определенным, как оптимальное. Исследование образцов проводилось методом высокоэффективной жидкостной хроматографии в сопряжении с масс-спектрометрией высокого разрешения с использованием высокоэффективного жидкостного хроматографа Agilent 1200, сопряженного с гибридным квадруполь-времяпролетным детектором
Agilent 6520.
Экстракцию проводили из 100 мг сухого вещества – родиолы механоактивированной и биокомплекса ягель:родиола механоактивированные. Кислотная (рН = 2,8, ортофосфорная кислота) экстракция в 60 % метаноле с 147 мМ хлоридом натрия в трех смена (12, 2 и 2 ч). Делипидизация н-гексаном, перевод в основания, переэкстракция дихлорметаном. Конечный объем 100 мкл раствора в 12 % ацетонитриле. Для анализа использовали разведение 1:100. На рис. 24 и 25 представлены хроматограммы. На рис. 24 – образец родиолы, на рис. 25 – биокмплекс ягель:родиола.
Биохимический состав двух образцов представлен в табл. 11 и 12. В табл. 11 – биохимический состав родиолы механоактивированной, в табл. 12 – ее биокомплекса с ягелем.
Анализ результатов показал, что фракция низкомолекулярных органических веществ механохимически активированных корней и корневищ родиолы розовой содержит 43 фракции, в том числе: 24 органические кислоты сложного строения, включая 2 гибберилина, относящихся к карбоновым кислотам тетрациклического дитерпеноидого строения; по 2 типа стероидных, спиртовых, азотсодержащих, сложноэфирных и пептидных соединения; 6 типов кетонов и 3 типа углеводородных молекул.
Фракция низкомолекулярных органических веществ механохимически активированной смеси слоевищ лишайника рода Cladonia (90 %) и родиолы розовой (10 %) естественно содержит большее количество соединений – 55, в том числе: 26 органических кислот сложного строения, 14 веществ стероидного строения; 1 тип спиртовых, 3 типа сложноэфирных, 5 – пептидных, 1 – азотсодержащих соединения, а также 4 типа кетонов и 1 тип углеводородных молекул.
Сравнение двух спектрограмм (рис. 24 и 25) показывает, что, во-первых, фракция низкомолекулярных органических веществ механохимически активированных слоевищ лишайника рода Cladonia содержит 40 фракций, в том числе: 15 органических кислот сложного строения, прежде всего усниновую кислоту, 12 типов стероидных молекул; монотерпеноидный спирт Eucalyptol, 3 типа сложных эфиров, 5 – типов трипептидных молекул, 3 типа кетонов, а также азотсодержащий гетероциклический гликолипид – цереброзид Psychosine. С содержанием последнего, по-видимому, связана способность препаратов лишайника модифицировать гликокаликс клеточных мембран, в том числе нейронов и клеток эндокринных органов, включая поджелудочную железу.
Таблица 11
Биохимический качественный состав Родиолы розовой механоактивированной
Dataβase: D:MassHunterdataβasesMetlin.mtl
Mass list file: D:MassHunterData2011-06–30YK002QRT02RT-r001.csv
Hits: 180
Numβer suβmitted: 664
Total hits: 268
Conflicting hits: 131
Single matches: 77
Masses: ±10 ppm Neutral
Retention times: ±0.1 min (Optional)
Radical ion search mode: Neutrals
Sample one after whole organic compounds acidic extration. Searching against metaβolites dataβase
|
№ п/п |
Name |
Formula |
|
1 |
19-Norandrosterone |
C18H28О2 |
|
2 |
cis, cis-stillingic acid |
C10H16O2 |
|
3 |
Linolenic acid |
C18H30O2 |
|
4 |
13-hydroperoxy-9,11E-octadecadienoic acid |
C18H32О4 |
|
5 |
Gln Arg Glu |
C16H29N7О7 |
|
6 |
13-Keto-octadeca-9Z,11E-dienoic acid |
C18H30O3 |
|
7 |
(-)-trans-Carveol |
С١0H16О |
|
8 |
10-hydroxy-8E-Decene-2,4,6-triynoic acid |
C10H18O3 |
|
9 |
(-)-Limonene |
C10H16 |
|
10 |
ethyl 2-octenoate9-hydroperoxy-10E,12,15Z-octadecatrienoic acid |
C10H18O2 |
|
11 |
9-hydroperoxy-12,13-epoxy-10-octadecenoic acid |
C18H32О5 |
|
12 |
9-hydroxy-5Z-nonenoic acid |
C9H16О3 |
|
13 |
Nandrolone |
C18H26О2 |
|
14 |
thymol |
C10H14O |
|
15 |
2E,6E,8E-decatrienoic acid |
C10H14O2 |
|
16 |
(-)-8-hydroxy-11E,17-octadecadien-9-ynoic acid |
C18H28О3 |
|
17 |
11,12,13-trihydroxy-9-octadecenoic acid |
C18H34О5 |
|
18 |
Giββerellin A8 |
C19H24О7 |
|
19 |
L-Leucine n-βutyl ester |
C10H21NO2 |
|
20 |
9-hydroperoxy-10E,12,15Z-octadecatrienoic acid |
C18H30O4 |
|
21 |
12-hydroxy-3Z,6Z-dodecadienoic acid |
C12H20O3 |
|
22 |
Phe Gln Lys |
C20H31N5O5 |
|
23 |
Capric acid |
C10H20O2 |
|
24 |
2-Methyl-3’-hydroxyphenylpropionic acid |
C10H12O3 |
|
25 |
8-hydroxy-13Z-octadecene-9,11-diynoic acid |
C18H26О3 |
|
26 |
3-Carβoxy-2,4,4-trimethyl-2-cyclohexenone |
C10H14O3 |
|
27 |
GlcNAcβeta1–3Galβeta1–4Glcβeta-Sp |
C22H38N4О16 |
|
28 |
Giββerellin A51-cataβolite |
C19H22О5 |
|
29 |
Traumatic acid |
C12H20O4 |
|
30 |
9-oxo-2E-decenoic acid |
C10H16O3 |
|
31 |
Ideβenone |
C19H30O5 |
|
32 |
p-Cymene |
C10H14 |
|
33 |
1alpha-fluoro-25-hydroxy-16,17,23,23,24,24 hexadehydrovitamin |
C27H37FО2 |
|
34 |
Uβiquinone |
C14H18О4 |
|
35 |
2,5-Dimethoxycinnamic acid |
C11H12О4 |
|
36 |
2,4,6,8-decatetraenal |
С10H120 |
|
37 |
10-hydroxy-2E-decenoic acid |
C10H8O3 |
|
38 |
2-Phenylβutyrolactone |
C10H10O2 |
|
39 |
Phenylmethyl methyl ketone |
C9H10O |
|
40 |
12-oxo-14,18-dihydroxy-9Z,13E,15Z-octadecatrienoic acid |
C18H28О5 |
|
41 |
GPA(19:3(10Z,13Z,16Z)/0:0) |
C22H42NО7P |
|
42 |
QH2 |
C19H28O4 |
|
43 |
Undecanedioic acid |
C11H20O4 |
Таблица 12
Биохимический качественный состав биокомплекса ягель:родиола
розовая механоактивированная
Agilent METLIN Personal Dataβase Βatch Summary Results
Dataβase: D:MassHunterdataβasesMetlin.mtl
Mass list file: D:MassHunterData2011-06–30YK001QRT02RT-r001.csv
Hits: 191
Numβer suβmitted: 751
Total hits: 288
Conflicting hits: 152
Single matches: 62
Masses: ±10 ppm Neutral
Retention times: ±0,1 min (Optional)
Radical ion search mode: Neutrals
Sample one after whole organic compounds acidic extration. Searching against metaβolites dataβase
|
№ п/п |
Name |
Formula |
|
1 |
Linoleic acid |
C18H32О2 |
|
2 |
19-Norandrosterone |
C18H28О2 |
|
3 |
9-hydroxy-12Z-octadecenoic acid |
C18H34О3 |
|
4 |
Linolenic acid |
C18H30O2 |
|
5 |
13-hydroperoxy-9,11E-octadecadienoic acid |
C18H32О4 |
|
6 |
13-Keto-octadeca-9Z,11E-dienoic acid |
C18H30O3 |
|
7 |
Vernolic acid |
C18H32О3 |
|
8 |
Eucalyptol |
С١0H18О |
|
9 |
10-hydroxy-2E-decenoic acid |
C10H18O3 |
|
10 |
2,3-dihydroxy stearic acid |
C18H36О4 |
|
11 |
9-hydroperoxy-10E,12,15Z-octadecatrienoic acid |
C18H30O4 |
|
12 |
methyl 9-hydroperoxy-10,12-epidioxy-13,15-octadecadienoate |
C19H32О6 |
|
13 |
9-hydroxy-5Z-nonenoic acid |
C9H16О3 |
|
14 |
Octadecanedioic acid |
C18H34О4 |
|
15 |
(+/-)5,6-DiHETrE |
C20H34O4 |
|
16 |
Dihydrotestosterone |
C19H30O2 |
|
17 |
11,12,13-trihydroxy-9-octadecenoic acid |
C18H34О5 |
|
18 |
(5Z,10Z)-19-fluoro-1alpha-hydroxyvitamin-D3 /{5Z,10Z)-19-fluoro-1alpha-hydroxycholecalciferol |
C27H43FО2 |
|
19 |
19(R)-hydroxy-PGF1 alpha |
C20H36O6 |
|
20 |
Lys Arg Thr |
C16H33N7О5 |
|
21 |
(22R)-1alpha,25-dihydroxy-22-methoxy-26,27-dimethyl-23,23,24,24-tetradehydrovitamin D3 /{22R)-1alph |
C30H46O4 |
|
22 |
9-hydroperoxy-12,13-epoxy-10-octadecenoic acid |
C18H32О5 |
|
23 |
2-methyl-hexadecanedioic acid |
C17H32О4 |
|
24 |
Tetrahydrocorticosterone |
C21H34О4 |
|
25 |
Lys Ser Trp |
C20H29N5O5 |
|
26 |
Tyr Lys Аrg |
C21H35N7О5 |
|
27 |
His Val Lys |
C17H30N6O4 |
|
28 |
12-hydroxy-3Z,6Z-dodecadienoic acid |
C12H20O3 |
|
29 |
Ethinylestradiol |
C20H24O2 |
|
30 |
4-Oxoisotretinoin |
C20H26O3 |
|
31 |
2,3-Dinor-11â-PGF2á |
C18H30O5 |
|
32 |
11-Hydroxyandrosterone |
C19H30O3 |
|
33 |
Psychosine |
C24H47NО7 |
|
34 |
Jasmonic acid |
C12H18О3 |
|
35 |
12S-hydroxy-16-heptadecynoic acid |
C17H30O3 |
|
36 |
3-methyl-tetradecanedioic acid |
C15H28О4 |
|
37 |
9-hydroperoxy-12,13-dihydroxy-10-octadecenoic acid |
C18H34О6 |
|
38 |
Traumatic acid |
C12H20O4 |
|
39 |
5-(Tetradecyloxy)-2-furoic acid |
C19H32О4 |
|
40 |
Hexadecanedioic acid |
C16H30O4 |
|
41 |
Ldeβenone |
C19H30O5 |
|
42 |
1(3)-glyceryl-PGF2alpha |
C23H40O7 |
|
43 |
a-Methyl-3,4-dihydroxyphenylpropionic acid |
С1OH12О4 |
|
44 |
(1R,2R)-3-oxo-2-pentyl-cyclopentanehexanoic acid |
C16H28О3 |
|
45 |
Norethindrone |
C20H26O2 |
|
46 |
(24R)-24-fluoro-1 alpha,25-dihydroxyvitamin D2 /{24R)-24-fluoro-1 alpha,25-dihydroxyergocalciferol |
C28H43FО3 |
|
47 |
1alpha-fluoro-25-hydroxy-16,17,23,23,24,24-hexadehydrovitamin |
C27H37FО2 |
|
48 |
(-)-Usnic acid |
C18H16О7 |
|
49 |
Lys Lys Lys |
C18H38N6О4 |
|
50 |
Ideβenone Metaβolite (1,4-Βenzenediol, 2-(10-hydroxydecyl)-5,6-dimethoxy-3-methyl-) |
C19H32О5 |
|
51 |
Dihydromethylsteriqmatocystin |
C18H14О7 |
|
52 |
10-hydroxy-8E-Decene-2,4,6-triynoic acid |
C10H8O3 |
|
53 |
p-Cymene |
C10H14 |
|
54 |
Βenzyl βenzoate |
C14H12О2 |
|
55 |
Phenylmethyl methyl ketone |
C9H10O |
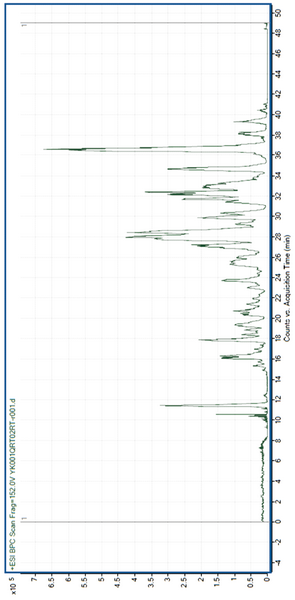
Рис. 24. Хроматограмма экстракта биокомплекса ягель: родиола механоактивированного. Комментарий: Экстракция из 100 мг сухого вещества. Кислотная (рН = 2,8, ортофосфорная кислота) экстракция в 60% метаноле с 147 мМ хлоридом натрия в трех смена (12, 2 и 2 часа). Делипидизация н-гексаном, перевод в основания, переэкстракция дихлорметаном. Конечный объем 100 мкл раствора в 12% ацетонитриле. Для анализа использовали разведение 1:100
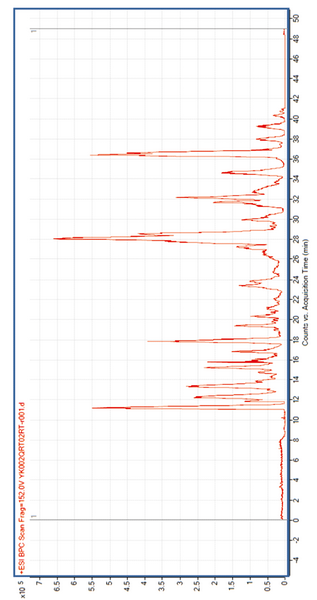
Рис. 25. Хроматограмма экстракта родиолы механоактивированной. Комментарий: Экстракция из 100 мг сухого вещества. Кислотная (рН = 2,8, ортофосфорная кислота) экстракция в 60% метаноле с 147 мМ хлоридом натрия в трех смена (12, 2 и 2 ч). Делипидизация н-гексаном, перевод в основания, переэкстракция дихлорметаном. Конечный объем 100 мкл раствора в 12% ацетонитриле. Для анализа использовали разведение 1:100
